Dans leur immense majorité (80%) les maladies rares sont d’origine génétique. Au sein de chacune de nos cellules nous possédons deux génomes distincts : le génome nucléaire (constitué des gènes contenus dans nos chromosomes) dont nous venons de parler ci-dessus, et le génome mitochondrial contenu dans les mitochondries (voir le dossier L’enfant aux trois parents). Nous allons voir dans ce qui suit les diverses causes de ces maladies. Mais il est tout d’abord nécessaire de rappeler brièvement les premières étapes de l’embryogénèse (figure ci-dessous).
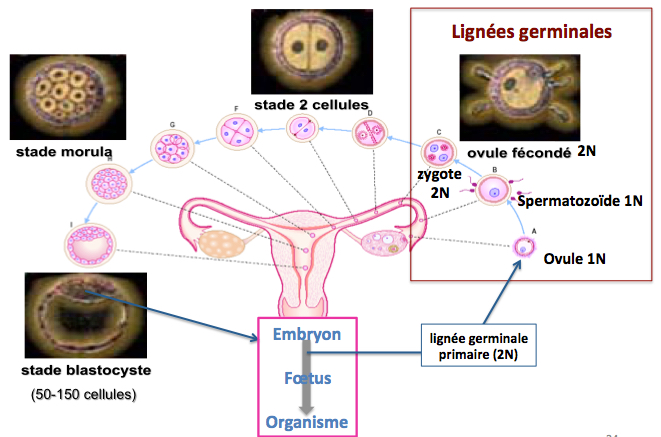
A chaque ovulation, un ovocyte est émis par l’ovaire. L’ovocyte est le gamette féminin et il comporte 23 chromosomes (on dit 1N chromosomes, c’est à dire qu’il n’y a qu’une seule copie de chaque chromosome), dont un chromosome sexuel, le chromosome X. Le gamette masculin est le spermatozoïde qui comporte également 23 chromosomes (1N chromosomes). A la différence de l’ovocyte, il y a deux types de spermatozoïdes, ceux dont le chromosome sexuel est un X et ceux dont le chromosome sexuel est un Y. Dans le zygote (l’embryon au stade une seule cellule) résultant de la fécondation de l’ovocyte par un spermatozoïde, on retrouve donc 1N chromosomes provenant de la mère et 1N chromosomes provenant du père (soient 2N chromosomes au total), et soit une combinaison XX des chromosomes sexuels (qui donnera une fille), soit une combinaison XY (garçon). Le zygote va ensuite se diviser pour passer à l’étape à 2 cellules, puis 4, 8, 16, 32, etc. cellules pour atteindre le stade du blastocyste qui va s’implanter dans la paroie de l’utérus. Le fetus va alors de développer. A noter que c’est au niveau de la masse cellulaire interne du blastocyste que sont prélevées les cellules souches embryonnaires.
Il existe plusieurs situations qui peuvent conduire à l’apparition d’une maladie d’origine génétique.
Maladies d'origine nucléaire
- mutation dans un gène nucléaire au niveau du zygote, cette mutation pouvant provenir soit de la copie du gène maternel (dans l’ovocyte) soit de la copie du gène paternel (spermatozoïde), soit des deux. On parle alors de transmission héréditaire ou Mendelienne.
- cette mutation peut avoir été transmise à la mère ou au père (ou aux deux) par l’un ou les deux de leurs ascendants.
- cette mutation peut être apparue spontanément dans les cellules souches des lignées germinales qui ont donné naissance au gamette (ovocyte ou spermatozoïde). On parle alors de mutation sporadique ou de novo, non héréditaire. Les parents n’en étaient pas porteurs.
- plus rarement, cette mutation peut être apparue spontanément dans le gamette (ovocyte ou spermatozoïde). Ici encore, on parle alors de mutation sporadique ou de novo, non héréditaire. Les parents n’en étaient pas porteurs.
- plus rarement encore, la mutation peut apparaître de novo au niveau du zygote ou ultérieurement dans une des cellules embryonnaires entre le stade zygote et le stade blastocyte ou plus tard dans les premières phase de développement du fetus. Dans ce cas, le phénomène de mosaïcisme peut apparaître (nous en parlerons dans un autre dossier).
Maladies d'origine mitochondriale
Les mitochondries sont des organelles cellulaires qui produisent l’ATP, le carburant de toutes les cellules (voir sur ce site L’enfant aux trois parents).
- mutation dans un gène mitochondrial, transmise exclusivement par la mère.
- cette mutation peut aussi apparaître spontanément pendant la vie fétale (ovogonies) ou dans l’ovocyte qui a donné naissance à l’enfant. Elle est dite alors sporadique ou de novo, non héréditaire, car non présente chez la mère.
- mutation dans un gène nucléaire qui code pour une protéine présente dans la mitochondrie et nécessaire à son fonctionnement.
Enfin, il faut préciser que toutes les mutations ne sont pas forcément pathologiques. Certaines peuvent être silencieuses et d’autres bénéfiques.
Transmission héréditaire ou Mendélienne
Nous avons vu précédemment que chaque embryon reçoit deux copies pour chacun de ses gènes, une provenant de la mère et une provenant du père. Chaque gène peut comporter une ou plusieurs mutation(s) dans sa séquence. On parle alors d’allèles du gène. C’est à dire que pour tout gène on peut trouver l’allèle normal (non muté, ou encore dit “sauvage”) ou l’allèle muté.
Chaque individu porte deux gènes (deux allèles). Il y a donc plusieurs possibilités :
- les deux allèles sont sauvages (non mutés) et l’individu est dit homozygote
- les deux allèles sont mutés et l’individu est homozygote pour cet allèle
- l’individu ne porte qu’un allèle muté et il est alors dit hétérozygote.
- l’individu porte deux allèles mutés mais différents (deux mmutation différentes dans le même gène) et il est dit hétérozygote.
Nous avons vu qu’une mutation dans la séquence d’un gène conduit à une mutation dans la protéine codée par ce gène. Dans la majorité des cas cette mutation conduira à la maladie. Ce sont évidemment les allèles mutés qui seront responsables des maladies génétiques.
Transmission autosomique récessive
Une transmission est dite autosomique lorsqu’elle concerne un gène situé sur un chromosome non sexuel (c’est à dire les chromosomes 1 à 22), et elle est dite récessive si la maladie nécessite la présence de deux allèles mutés pour s’exprimer. C’est à dire que seuls les homozygotes pour l’allèle muté sont malades. Un exemple est donné dans la figure ci-dessous.
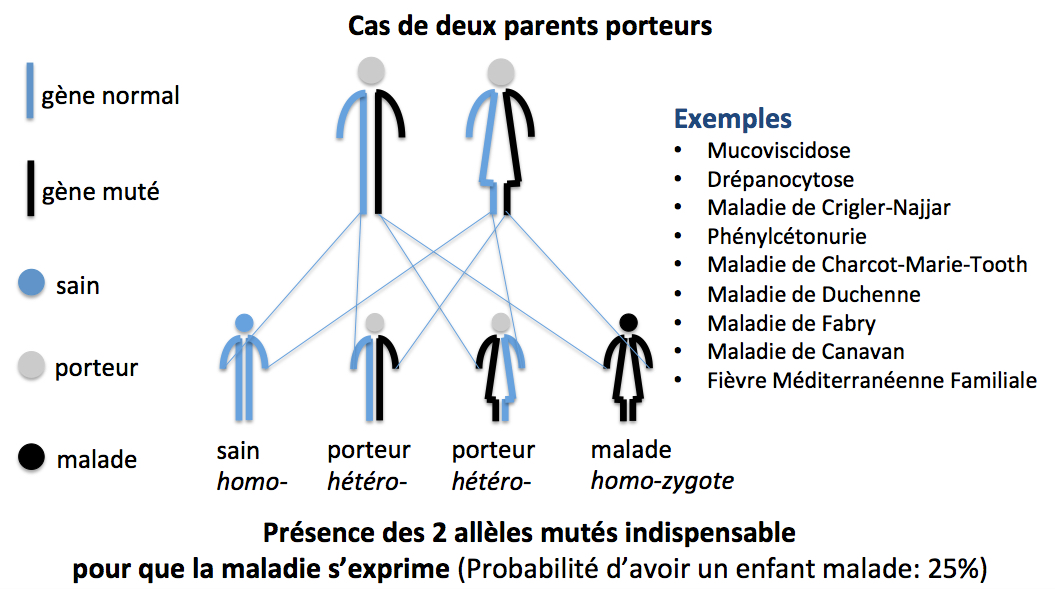
Dans cet exemple, les deux parents sont porteurs sains (non malades), ils sont hétérozygotes pour l’allèle muté du gène concerné. Les quatre combinaisons possibles donnent :
- un enfant homozygote pour l’allèle sauvage (non muté) non malade,
- deux enfants hétérozygotes pour l’allèle muté non malades,
- un enfant homozygote pour l’allèle muté et donc malade.
Pour ce couple donc, la probabilité d’avoir un enfant malade est de 25%.
Il existe d’autres possibilités :
- un seul parent est porteur de la mutation et non malade. Il est donc hétérozygote pour l’allèle muté. Ce couple engendrera 50% d’enfant hétérozygotes pour l’allèle muté mais aucun malade.
- un parent est malade (homozygote pour l’allèle muté) et l’autre parent sain non porteur (homozygote pour l’allèle “sauvage”) : pas d’enfant malade mais 100% d’hétérozygotes.
- un parent est malade (homozygote pour l’allèle muté) et l’autre est porteur de l’allèle muté mais sain (hétérozygote). Dans ce cas 50% des enfants sont hétérozygotes et 50% sont homozygotes pour l’allèle muté et donc malades.
- les deux parents sont malades (homozygotes pour l’allèle muté) : 100 des enfants sont malades.
Dans le cas des maladies génétiques à transmission autosomique récessive, la mutation fait perdre à la protéine concernée une partie importante (ou la totalité) de sa fonction. Chez les hétérozygotes, cette fonction est assurée par la protéine (normale) issue de l’allèle non muté et la maladie ne s’exprime pas (ou parfois elle s’exprime à un bas niveau). En revanche, la maladie s’exprimera chez les homozygotes pour l’allèle muté avec une forte (ou totale) perte de fonction de la protéine concernée. C’est typiquement le cas du canal chlorure (CFRT) dans la mucoviscidose que je traiterai plus loin.
Transmission autosomique dominante
Une transmission est dite dominante lorsqu’un seul allèle muté suffit pour que la maladie s’exprime. C’est à dire que tous les hétérozygotes sont malades. Un exemple est donné dans la figure ci-dessous.
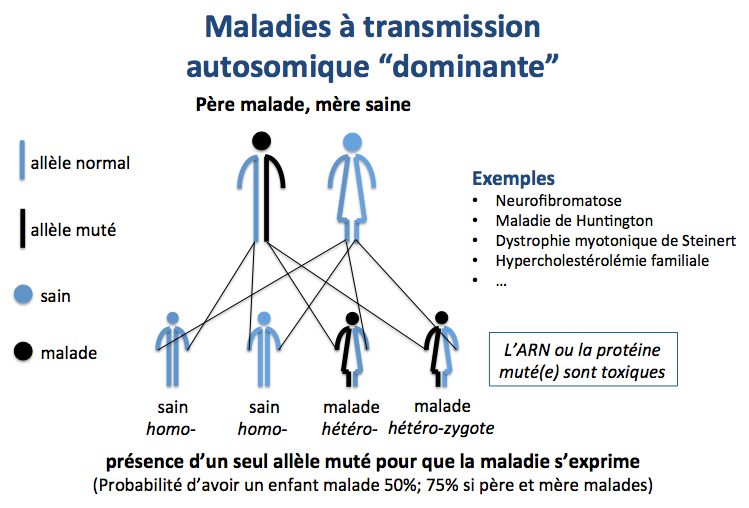
Dans cet exemple, un parent est porteur d’un allèle muté et donc malade, l’autre parent est sain (homozygote pour l’allèle sauvage). Les combinaisons possibles donnent :
- deux enfants hétérozygotes pour l’allèle muté et donc malades,
- deux enfants homozygotes pour l’allèle sauvage et donc non malades.
Pour ce couple donc, la probabilité d’avoir un enfant malade est de 50%.
Il existe d’autres possibilités :
- les deux parents sont malades (hétérozygotes pour l’allèle muté) : 75% des enfants sont malades.
- un parent est homozygote pour l’allèle muté, 100% des enfants sont malades.
- les deux parents sont homozygotes pour l’allèle muté, 100% des enfants sont malades.
Dans le cas de ces maladies génétiques à transmission autosomique dominante, la sévérité de la maladie est en général fortement augmentée chez les homozygotes. De plus, il semble que la protéine responsable acquiert du fait de la mutation non pas une déficience, c’est à dire une perte plus ou moins importante de son activité normale, mais plutôt une modification de sa fonction normale qui lui confère une fonction “toxique”. C’est typiquement le cas de la huntingtine dans la maladie de Huntington que je traiterai plus loin. Il existe également des cas où l'ARN muté est lui-même toxique (Dystrophie myotonique de Steinert).
Le chromosome X et les différences sexuelles en termes de santé
Nous avons vu ci-dessus les cas de maladies consécutives à une mutation sur un gène porté par les chromosomes non sexuels c’est à dire les chromosomes 1 à 22. Il reste le cas d’un gène muté dans les chromosomes sexuels X ou Y.
Aucun gène vital ne réside sur le chromosome Y puisque les femmes en sont dépourvues. Ce chromosome ne comporte qu’une centaine de gènes spécifiquement impliqués dans le développement “mâle”. Les maladies liées au chromosome Y affectent donc le développement sexuel masculin, notamment le développement testiculaire (gène impliqué, SRY), la fertilité, les troubles de la spermatogénèse (nombre réduit des spermatozoïdes). Une forte déficience de l’Y conduit à un phénotype féminin.
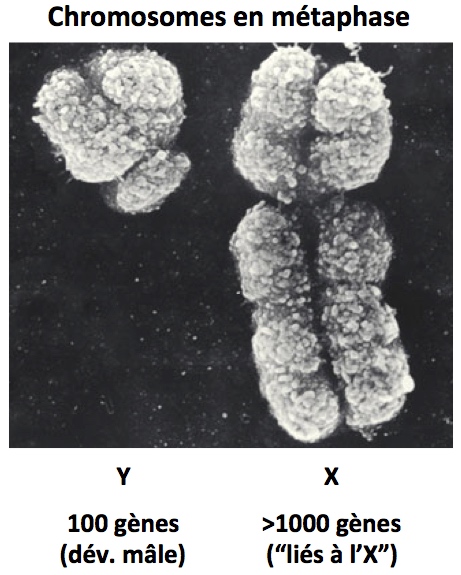
La femme possède deux chromosomes X et l’homme, un chromosome X et un chromosome Y. A l’inverse du chromosome Y, le chromosome X porte plus de mille gènes. Ces gènes sont dits “liés à l’X”. Dans les cas de mutations dans un gène porté par l’X, l’homme est plus vulnérable que la femme. En effet, si un gène est muté dans l’X chez la femme, sa fonction peut être supléée par la copie non mutée présente sur l’autre X. Chez la femme, un des deux chromosomes X est inactivé, mais cette inactivation se fait au hasard. Statistiquement donc, le chromosome X portant la mutation a une chance sur deux d’être inactivé de sorte que le gène non muté présent sur l’autre X est exprimé et il n’y a généralement pas de pathologie. Une mutation sur un gène lié à l’X chez l’homme conduit fatalement à la pathologie correspondante, comme par exemple la dystrophie musculaire de Duchenne, le syndrome de l’X fragile, etc. Ces maladies sont dites liées à l’X.
Il existe entre 7 et 8000 maladies rares répertoriées, comme indiqué en introduction. L’objet de ce site n’est pas de les décrire toutes. Je conseille au lecteur intéressé par une maladie rare particulière de consulter les sites spécialisés, comme par exemple Orphanet (http://www.orphanet-france.fr/), ou (en anglais) le GARD (Genetic And Rare Diseases Information Center) (https://rarediseases.info.nih.gov).
Je vais traiter dans ce site seulement quelques cas dans lesquels la maladie résulte de mécanismes moléculaires et biologiques très différents: mucoviscidose, maladie de Huntington, syndrome de Rett (à venir), progéria (à venir) et d'autres... A suivre.
N'hésitez pas à me contacter (patrick.maurel@inserm.fr) si vous avez des questions, commentaires, critiques, ou souhaitez faire part d'une expérience personnelle. Je vous répondrai aussi rapidement que possible.