Epidermolyse bulleuse jonctionnelle
La régénération de l’épiderme a déjà été utilisée dans le cadre du traitement de malades atteints de maladies génétiques ou après des traumatismes tels que les brûlures.
Un article récemment publié dans Nature par un consortium international Allemand, Italien et Autrichien dirigé par le Dr Michele De Luca (Hirsch et al. Nature 2017, Regeneration of the entire human epidermis using transgenic stem cells) vient de montrer la régénération épidermique à large échelle chez un enfant de 7 ans atteint d’épidermolyse bulleuse jonctionnelle. Cette maladie génétique rare est souvent mortelle (40% des cas). Chez cet enfant le pronostoc vital était engagé du fait de la sévérité de sa maladie. Après avoir reçu un greffe de peau à large échelle sur tout son corps (0,8 m2), il a retrouvé non seulement une peau nourmale, mais il est en bonne santé, un an après l’intervention. Le point très intéressant et novateur de cet article est qu’il a montré le rôle central des cellules souches dans la régénération et l’homéostase de l’épiderme.
L’enfant est porteur d’une mutation dans le gène LAMB3
Cette mutation (C1977-1G>A, IVS 14-1G>A, dans l'intron 14) affecte l’épissage de l’ARN messager, et conduit à l’absence de la protéine codée par ce gène, la laminine 322 qui assure la jonction entre le derme et l’épiderme. Il se créé de ce fait chez ces malades des bulles, cloques emplies de liquide interstitiel, entre le derme et l’épiderme. Cette maladie se caractérise également par une augmentation du risque de cancers de la peau. L’idée était donc de remplacer l’épiderme déficient par des cellules épidermiques ayant été génétiquement modifiées pour exprimer le gène LAMB3 normal avec l’espoir que ce traitement pourrait restaurer une peau normale chez le malade. Le pronostic vital de l’enfant était engagé car il avait perdu juste avant l’intervention 60% de son épiderme, la perte globale atteignant un niveau de 80%.
Thérapie génique et cellulaire
Les chercheurs ont prélevé 0,4 cm2 de peau sur une zône non encore touchée et ont réalisé à partir de cette biopsie une culture de cellules. Après une pousse suffisante, ces cellules ont été transfectées avec un virus modifié de la leucémie Murine exprimant le gène LAMB3 normal. A noter que le gène muté n’a pas été remplacé mais a simplement été suppléé par le gène normal, ce dernier rétablissant la fonction perdue (production de laminine 322).
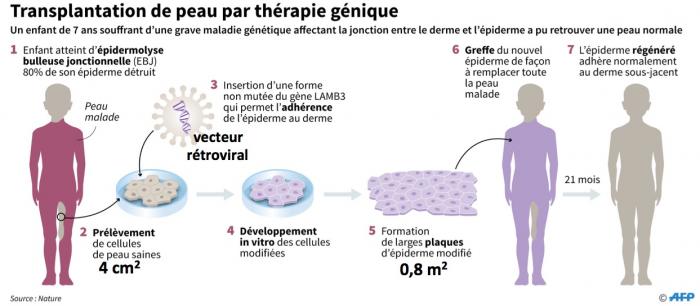
Ce shéma (source AFP) résume la procédure.
Des plaques de cellules épidermiques exprimant le gène normal ont alors été greffées sur le coprs de l’enfant et ont permis la restauration de son épiderme. Cette étude est importante dans la mesure où elle combine une thérapie génique et une thérapie cellulaire de la peau, de façon similaire à ce qui a déjà été utilisé dans le cadre de traitements de maladies hématopoïétiques (cellules du sang).
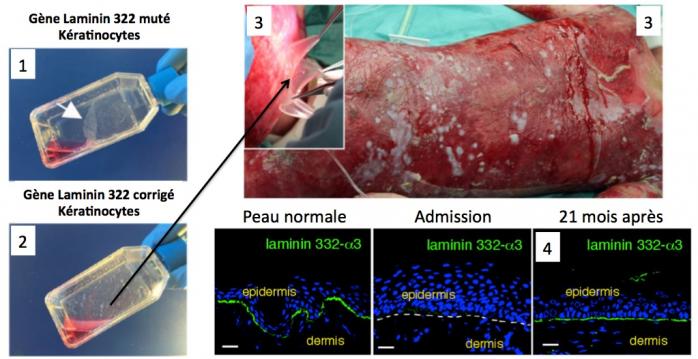
Cette figure (source l'article de Hirsch, Nature 2017; extended Figures 2 and 3) montre certains résultats. 1: les kératinocytes du malade ne s'accrochent pas au flacon de culture (flêche blanche) du fait de l'absence de laminine 322 (gène LAMB3 muté); 2: après transfection de ces cellules avec le vecteur rétroviral exprimant le gène LAMB3 normal ce défaut disparaît; 3: Ces cellules ont été cultivées suffisamment pour produire 0,8m2 de plaques épidermiques qui ont été greffées sur le corps de l'enfant; 4: l'analyse de biopsies de peau est présentée ici: à gauche peau normale, la laminine 322 est révélée entre derme et épiderme par des anticorps marqués avec un fluorochrome vert; au centre et à droite, peau de l'enfant à son admission (pas de laminine 322) et 21 mois après l'intervention montrant l'expression de la laminine 322 dans la zône de jonction entre derme et épiderme.
Il s’agit d’un premier traitement dont le résultat est clairement spectaculaire et encourageant, mais dont les risques ne sont pas à négliger.
Pourquoi ?
· Le rétrovirus utilisé est susceptible (comme tous les rétrovirus) d’intégrer son génome dans des locus génétiques dont la fonction est importants (oncogènes, ou gènes inactivateurs de tumeurs), favorisant ainsi l’apparition de cancers.
· Surexpression de LAMB3 dont on ignore les conséquences à long terme.
· Il est possible que les clônes cellulaires du nouvel épiderme s’épuisent dans leur prolifération au cours du temps. En effet la peau est un tissu très dynamique dont le temps de renouvellement est court (de l’ordre du mois).
· Il est aussi possible que l’expression du gène normal transfecté diminue au cours du temps. Si cela devait arriver il faudrait envisager de conserver des cellules corrigées du malade afin de les lui greffer à nouveau.
Il sera donc important de suivre cet enfant de façon très rigoureuse durant les prochaines années
Malgré ces risques, cette procédure pourrait être utilisée chez les milliers de malades atteints par l’épidermolyse bulleuse jonctionnelle dans les cas où la maladie est potentiellement mortelle. Il s’agira donc pour les médecins et les familles de décider si le rapport bénéfice/risque est suffisant pour que cette thérapie soit entreprise.