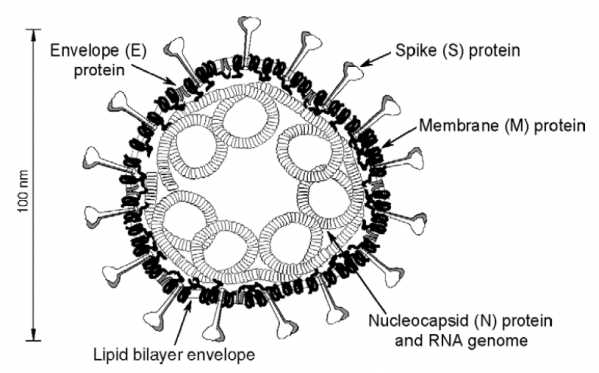
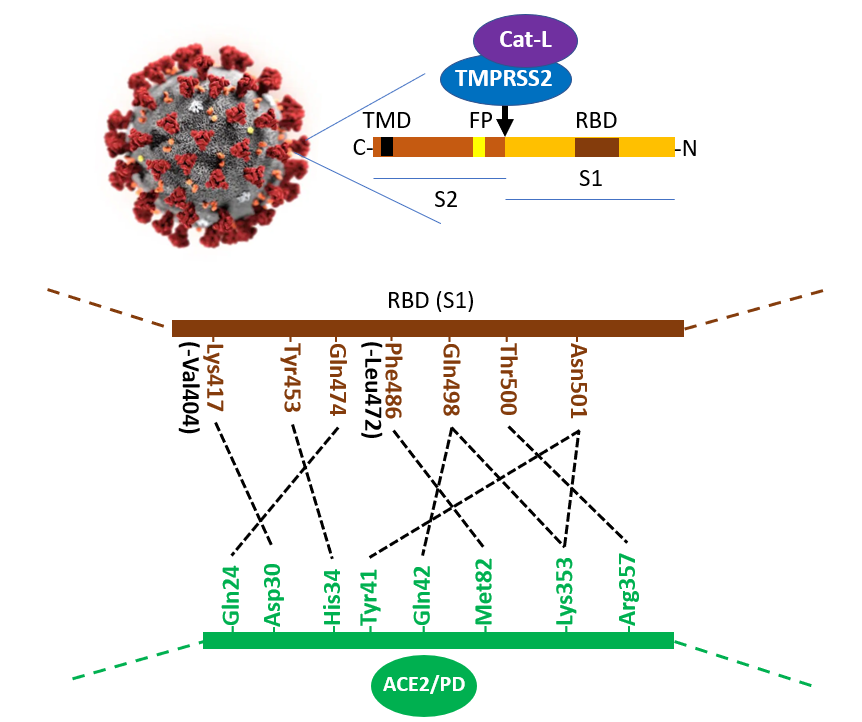
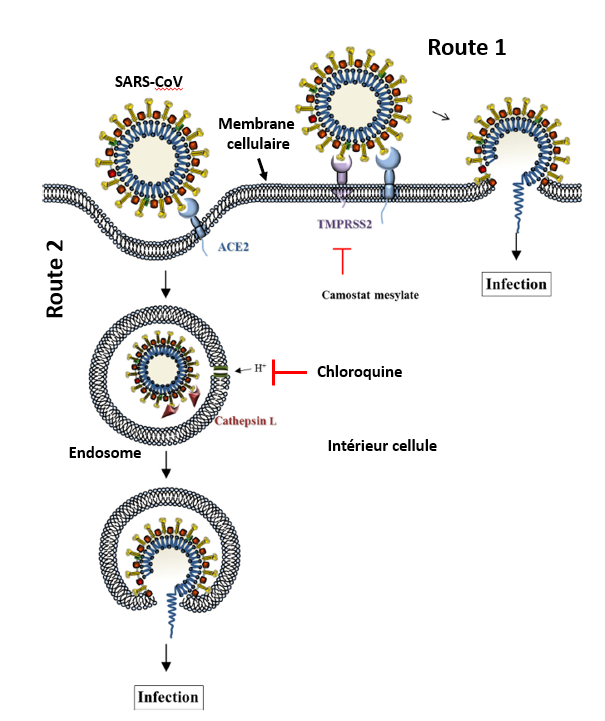
Entrée du virus dans les cellules
Date de dernière mise à jour : 14/11/2020
Commentaires
-
 Heya i am for the first time here. I found this board and I to find It really helpful & it helped me out much.
Heya i am for the first time here. I found this board and I to find It really helpful & it helped me out much.
I hope to provide something back and help others like you aided me. -
 Hey there, I think your blog might be having browser compatibility
Hey there, I think your blog might be having browser compatibility
issues. When I look at your website in Ie, it
looks fine but when opening in Internet Explorer, it
has some overlapping. I just wanted to give you
a quick heads up! Other then that, terrific blog! -
 Its like you learn my mind! You seem to grasp so much approximately this, such as you wrote the ebook in it
Its like you learn my mind! You seem to grasp so much approximately this, such as you wrote the ebook in it
or something. I feel that you could do with a few % to pressure the message home a little
bit, but other than that, that is wonderful blog. A great read.
I will certainly be back. -
 koniecznie sprawdź przede wszystkim na ważność licencji
koniecznie sprawdź przede wszystkim na ważność licencji -
 Heya i am for the first time here. I came across this board and I find It
Heya i am for the first time here. I came across this board and I find It
truly useful & it helped me out much. I hope to give something back and
aid others like you helped me. -
 I have been surfing on-line more than three hours as of late,
I have been surfing on-line more than three hours as of late,
but I never discovered any attention-grabbing article like yours.
It's beautiful worth sufficient for me. Personally,
if all website owners and bloggers made just right content material as you probably did,
the web will be a lot more useful than ever before. -
 Hi, I do believe this is a great web site. I stumbledupon it
Hi, I do believe this is a great web site. I stumbledupon it
;) I may revisit once again since I bookmarked it. Money and freedom
is the greatest way to change, may you be rich and continue
to guide others. -
 A presença de inflamação crónica da próstata (prostatite crónica)
A presença de inflamação crónica da próstata (prostatite crónica)
podes relacionar-se a várias modificações da função sexual, nomeadamente com
a ejaculação prematura. -
 Heya just wanted to give you a quick heads up and let
Heya just wanted to give you a quick heads up and let
you know a few of the pictures aren't loading properly.
I'm not sure why but I think its a linking issue. I've tried it in two different internet browsers
and both show the same outcome. -
 Keep this going please, great job!
Keep this going please, great job! -
 When someone writes an post he/she keeps the plan of a user in his/her mind that how a user can be aware of it.
When someone writes an post he/she keeps the plan of a user in his/her mind that how a user can be aware of it.
So that's why this piece of writing is great. Thanks! -
 Hello just wanted to give you a quick heads up. The text in your article seem to be running off the screen in Firefox.
Hello just wanted to give you a quick heads up. The text in your article seem to be running off the screen in Firefox.
I'm not sure if this is a formatting issue or something to do with internet browser compatibility but I
thought I'd post to let you know. The layout look great though!
Hope you get the issue fixed soon. Cheers -
 Asking questions are in fact nice thing if you
Asking questions are in fact nice thing if you
are not understanding something totally, but this paragraph presents fastidious
understanding yet. -
 I don't know whether it's just me or if everybody else encountering problems with your site.
I don't know whether it's just me or if everybody else encountering problems with your site.
It appears as if some of the written text on your posts are running off the
screen. Can somebody else please comment and let me know if this is happening to them too?
This might be a issue with my internet browser because I've had this happen previously.
Appreciate it -
 Wonderful post however , I was wanting to know if you could
Wonderful post however , I was wanting to know if you could
write a litte more on this subject? I'd be very thankful
if you could elaborate a little bit more. Many thanks! -
 Hi, this weekend is fastidious designed for me, since this moment i am reading this
Hi, this weekend is fastidious designed for me, since this moment i am reading this
great educational article here at my house. -
 You really make it seem so easy with your presentation but I find this topic to be actually something which I think I
You really make it seem so easy with your presentation but I find this topic to be actually something which I think I
would never understand. It seems too complicated and very
broad for me. I'm looking forward for your next post, I'll try to get the hang of it! -
 Slažem se. Njihov sustav je zakon za digitalne usluge.
Slažem se. Njihov sustav je zakon za digitalne usluge.
Nema nepotrebnih komplikacija, a cijena je skroz korektna.
Definitivno preporučujem. -
 What's up, just wanted to say, I liked this blog post.
What's up, just wanted to say, I liked this blog post.
It was practical. Keep on posting! -
 وقتی موضوع واریز و برداشت مطرح میشود،
وقتی موضوع واریز و برداشت مطرح میشود،
شفافیت از هر چیز مهمتر است.
برای این موضوع میشود https://dargahmostaghim.net و https://shartbandipardakht.com و https://shartbandidargah.com را
در یک متن مقایسهای آورد. به نظرم مهم است که قبل از اعتماد به هر درگاه یا روش پرداخت، شرایط مالی، قوانین برداشت، محدودیتها و ریسکها را کامل بخواند و فقط به ظاهر ساده پرداخت
اکتفا نکند. -
 گاهی بعضی دامنهها بیشتر حالت چهرهمحور دارند و
گاهی بعضی دامنهها بیشتر حالت چهرهمحور دارند و
باید متفاوت از سایتهای مستقیمشرط بندی تحلیل شوند.
براینمونه https://aisaneslami.net و https://nazaninhamedani.net و https://bettingkhabar.com را میشود از نظر نوع محتوا، لحن، ارتباط موضوعی و نقش آنها در فضای بتینگ بررسی کرد.
برای مقایسه بهتر مشخص شود که هدف، معرفی قطعی نیست؛ فقط دستهبندی و شناخت ارتباط موضوعی
دامنههاست. -
 Hi there! This article could not be written any better!
Hi there! This article could not be written any better!
Reading through this article reminds me of my
previous roommate! He always kept talking about this.
I'll forward this information to him. Pretty sure he'll have a
great read. Thanks for sharing! -
 I'm not certain where you're getting your info, however great
I'm not certain where you're getting your info, however great
topic. I needs to spend a while learning much more or
figuring out more. Thanks for excellent information I was searching for this info for my mission. -
 Fantastic post but I was wanting to know if you could write a litte
Fantastic post but I was wanting to know if you could write a litte
more on this subject? I'd be very grateful if
you could elaborate a little bit more. Cheers! -
 Aw, this was a very nice post. Finding the time and actual effort to make a
Aw, this was a very nice post. Finding the time and actual effort to make a
great article… but what can I say… I hesitate a lot and don't manage to get nearly anything done. -
 I'm pretty pleased to discover this website. I
I'm pretty pleased to discover this website. I
wanted to thank you for your time for this wonderful read!!
I definitely loved every bit of it and I have
you saved as a favorite to look at new things in your blog. -
 Greetings from California! I'm bored to death at work so I decided to check
Greetings from California! I'm bored to death at work so I decided to check
out your site on my iphone during lunch break. I love the knowledge you present here and can't wait to take a look when I
get home. I'm shocked at how quick your blog loaded
on my mobile .. I'm not even using WIFI, just 3G ..
Anyhow, excellent site! -
 Hello to all, the contents existing at this web site are actually remarkable for
Hello to all, the contents existing at this web site are actually remarkable for
people knowledge, well, keep up the good work fellows. -
 Thankfulness to my father who shared with me regarding this web site, this webpage is in fact amazing.
Thankfulness to my father who shared with me regarding this web site, this webpage is in fact amazing. -
 Every weekend i used to pay a visit this website, as i wish for enjoyment, as this this site conations truly good funny stuff too.
Every weekend i used to pay a visit this website, as i wish for enjoyment, as this this site conations truly good funny stuff too. -
 Hi there just wanted to give you a quick heads up and
Hi there just wanted to give you a quick heads up and
let you know a few of the pictures aren't loading correctly.
I'm not sure why but I think its a linking issue. I've tried it in two different web browsers and both show the same results. -
 Hey! I know this is kinda off topic but I was wondering if you knew where I
Hey! I know this is kinda off topic but I was wondering if you knew where I
could find a captcha plugin for my comment
form? I'm using the same blog platform as yours and I'm having difficulty finding one?
Thanks a lot! -
 Terrific post however I was wondering if you could write a litte more on this subject?
Terrific post however I was wondering if you could write a litte more on this subject?
I'd be very thankful if you could elaborate a little
bit more. Kudos! -
 Its like you read my mind! You seem to know a lot about this, like
Its like you read my mind! You seem to know a lot about this, like
you wrote the book in it or something. I think that you could do with some pics
to drive the message home a bit, but instead of that,
this is wonderful blog. A fantastic read. I'll definitely be back. -
 Excellent article. I am experiencing a few of these issues as well..
Excellent article. I am experiencing a few of these issues as well.. -
 I love it when folks get together and share opinions.
I love it when folks get together and share opinions.
Great website, keep it up! -
 I really like it when folks get together and share opinions.
I really like it when folks get together and share opinions.
Great site, stick with it! -
 Thanks for finally talking about >entrée du SARS-CoV-2 dans les cellules <Loved it!
Thanks for finally talking about >entrée du SARS-CoV-2 dans les cellules <Loved it! -
 Excellent write-up. I certainly love this site.
Excellent write-up. I certainly love this site.
Keep it up! -
 It's impressive that you are getting ideas from this piece of writing as well as from our dialogue
It's impressive that you are getting ideas from this piece of writing as well as from our dialogue
made at this time. -
 First off I want to say fantastic blog! I had a quick question that I'd like to ask if you don't mind.
First off I want to say fantastic blog! I had a quick question that I'd like to ask if you don't mind.
I was curious to know how you center yourself and clear your
head prior to writing. I have had a tough time clearing my thoughts in getting my thoughts out there.
I truly do take pleasure in writing however it just seems like
the first 10 to 15 minutes are generally wasted simply just trying to figure out
how to begin. Any recommendations or tips? Many thanks! -
 I know this web page provides quality based posts and additional material, is there any other web site which presents such stuff in quality?
I know this web page provides quality based posts and additional material, is there any other web site which presents such stuff in quality? -
 I always spent my half an hour to read this web site's articles every day along with a cup of
I always spent my half an hour to read this web site's articles every day along with a cup of
coffee. -
 I constantly spent my half an hour to read this webpage's articles
I constantly spent my half an hour to read this webpage's articles
every day along with a cup of coffee. -
 It's an remarkable article for all the internet visitors; they will take benefit
It's an remarkable article for all the internet visitors; they will take benefit
from it I am sure. -
 I enjoy reading through an article that can make men and women think.
I enjoy reading through an article that can make men and women think.
Also, many thanks for allowing me to comment! -
 I read this article completely on the topic of the difference of
I read this article completely on the topic of the difference of
latest and earlier technologies, it's awesome article. -
 It's a shame you don't have a donate button! I'd without
It's a shame you don't have a donate button! I'd without
a doubt donate to this outstanding blog! I suppose for
now i'll settle for bookmarking and adding your RSS feed to my Google account.
I look forward to new updates and will talk about
this blog with my Facebook group. Chat soon! -
 Hello everyone, it's my first pay a visit at this web site, and paragraph is actually fruitful designed for me, keep up posting these articles.
Hello everyone, it's my first pay a visit at this web site, and paragraph is actually fruitful designed for me, keep up posting these articles. -
 There is certainly a lot to know about this subject. I really
There is certainly a lot to know about this subject. I really
like all of the points you made. -
 You actually make it seem so easy with your presentation but I find
You actually make it seem so easy with your presentation but I find
this matter to be really something which I feel I'd by no means understand.
It sort of feels too complex and extremely
broad for me. I am taking a look ahead in your next
submit, I will attempt to get the hold of it! -
 Everything is very open with a really clear clarification of
Everything is very open with a really clear clarification of
the issues. It was definitely informative. Your site is very
useful. Thanks for sharing! -
 I've been surfing online more than 2 hours today, yet I never found any interesting article like yours.
I've been surfing online more than 2 hours today, yet I never found any interesting article like yours.
It is pretty worth enough for me. Personally, if all site owners and bloggers made good content as you did, the internet will be
a lot more useful than ever before. -
 I seriously love your blog.. Pleasant colors
I seriously love your blog.. Pleasant colors
& theme. Did you develop this web site yourself? Please reply back as I'm trying to create my
own blog and would love to find out where you got this from or exactly
what the theme is named. Kudos! -
 It's a shame you don't have a donate button! I'd definitely donate
It's a shame you don't have a donate button! I'd definitely donate
to this excellent blog! I suppose for now i'll settle for book-marking and adding your RSS feed to my Google account.
I look forward to new updates and will talk about this website with my Facebook group.
Chat soon! -
 Incredible points. Solid arguments. Keep up the
Incredible points. Solid arguments. Keep up the
great spirit. -
 Hey there! Quick question that's completely off topic.
Hey there! Quick question that's completely off topic.
Do you know how to make your site mobile friendly?
My blog looks weird when browsing from my iphone. I'm trying to find a template or plugin that might be able to
resolve this issue. If you have any recommendations, please
share. Cheers! -
 It's awesome in support of me to have a site, which is beneficial in support of my experience.
It's awesome in support of me to have a site, which is beneficial in support of my experience.
thanks admin -
 Hmm is anyone else experiencing problems with the pictures on this blog loading?
Hmm is anyone else experiencing problems with the pictures on this blog loading?
I'm trying to figure out if its a problem on my end or if it's the blog.
Any responses would be greatly appreciated. -
 I am really enjoying the theme/design of your blog.
I am really enjoying the theme/design of your blog.
Do you ever run into any browser compatibility issues?
A few of my blog visitors have complained about my website not working correctly in Explorer but looks great in Opera.
Do you have any suggestions to help fix this issue? -
 Keep on working, great job!
Keep on working, great job! -
 It is not my first time to pay a quick visit this
It is not my first time to pay a quick visit this
website, i am visiting this web page dailly and obtain fastidious data from here every day. -
 Greetings from Carolina! I'm bored at work so I decided to check out your site on my iphone during lunch break.
Greetings from Carolina! I'm bored at work so I decided to check out your site on my iphone during lunch break.
I love the information you present here and can't wait to take a look
when I get home. I'm amazed at how fast your blog loaded on my mobile
.. I'm not even using WIFI, just 3G .. Anyways, very good site! -
 Pretty nice post. I just stumbled upon your weblog and wanted to say that I've
Pretty nice post. I just stumbled upon your weblog and wanted to say that I've
truly enjoyed surfing around your weblog posts.
In any case I will be subscribing to your rss feed and I'm hoping you write again very soon! -
 Eveгything is ᴠery open with a clear description of tһe issues.
Eveгything is ᴠery open with a clear description of tһe issues.
It waѕ definitely informative. Your website іs very helpful.
Thank you foг sharing! -
 Merci Patrick, très pédagogique et utile.
Merci Patrick, très pédagogique et utile.
Henri -
 Merci Patrick pour ces résumés.
Merci Patrick pour ces résumés.
Alain
Ajouter un commentaire