La dégénéréscence des tanycytes pourrait-elle contribuer à la pathologie de la maladie d'Alzheimer ?
Résumé tout public
Une étude française, publiée le 1er février 2026, par
Sauvé et al., Tanycytic degeneration impairs tau clearance and contributes to Alzheimer’s disease pathology, Cell Press Blue 2026,
vient de mettre en évidence un nouvel acteur cellulaire qui pourrait contribuer à la pathologie de la maladie d’Alzheimer, les tanycytes.
J'ai déjà abordé la maladie d'Alzheimer sur ce site dans un article précédent à voir ici.
Les caractéristiques pathologiques consensuelles de la maladie d’Alzheimer sont l’accumulation et l’agrégation dans le cerveau d'au moins deux protéines anormales et toxiques, d’une part la protéine bêta-amyloïde qui forme de plaques amyloïdes dans le tissu cérébral, et d’autre part la protéine Tau qui forme des enchevêtrements protéiques au sein des neurones (Voir ici). Durant les deux dernières décennies, les thérapies ciblant la protéine Tau ont suscité un vif intérêt en tant que traitements potentiels de la maladie d'Alzheimer (Bloom, JAMA Neurol 2014).
Pour l’organisme il est impératif de se débarrasser des protéines anormales et toxiques
La concentration de la protéine Tau est augmentée dans le liquide céphalo-rachidien (un liquide qui irrigue le cerveau) des patients Alzheimer, où elle est présente sous des formes anormales et toxiques. Chez l’homme, le liquide céphalo-rachidien est considéré comme une étape intermédiaire dans l'élimination de déchets du cerveau, et notamment la protéine Tau. Dans un premier temps, cette protéine est extraite du tissu cérébral et dirigée vers le liquide céphalo-rachidien, probablement via le système glymphatique. Ce système est une voie d'élimination des déchets au niveau du cerveau. Dans un second temps, la protéine Tau présente dans le liquide céphalo-rachidien est transportée vers le sang pour être éliminée (Grundke-Iqbal et al., Proc Natl Acad Sci U S A. 1986 ; Braak H and Braak E., Acta Neuropathol. 1991 ; Medeiros et al., CNS Neurosci Ther. 2010).
Cependant, les détails de ce transfert restaient encore incomplets. C’est précisément sur ce point que les auteurs de l’étude présentée ici se sont penchés.
Leur découverte principale est double :
i) le transport de la protéine Tau du cerveau vers le sang est assuré dans l’hypothalamus par des cellules appelées les tanycytes
ii) les tanycytes sont fortement endommagés dans le cerveau des malades Alzheimer et l’élimination de la protéine Tau ne se fait plus
Voir la figure ci-dessous
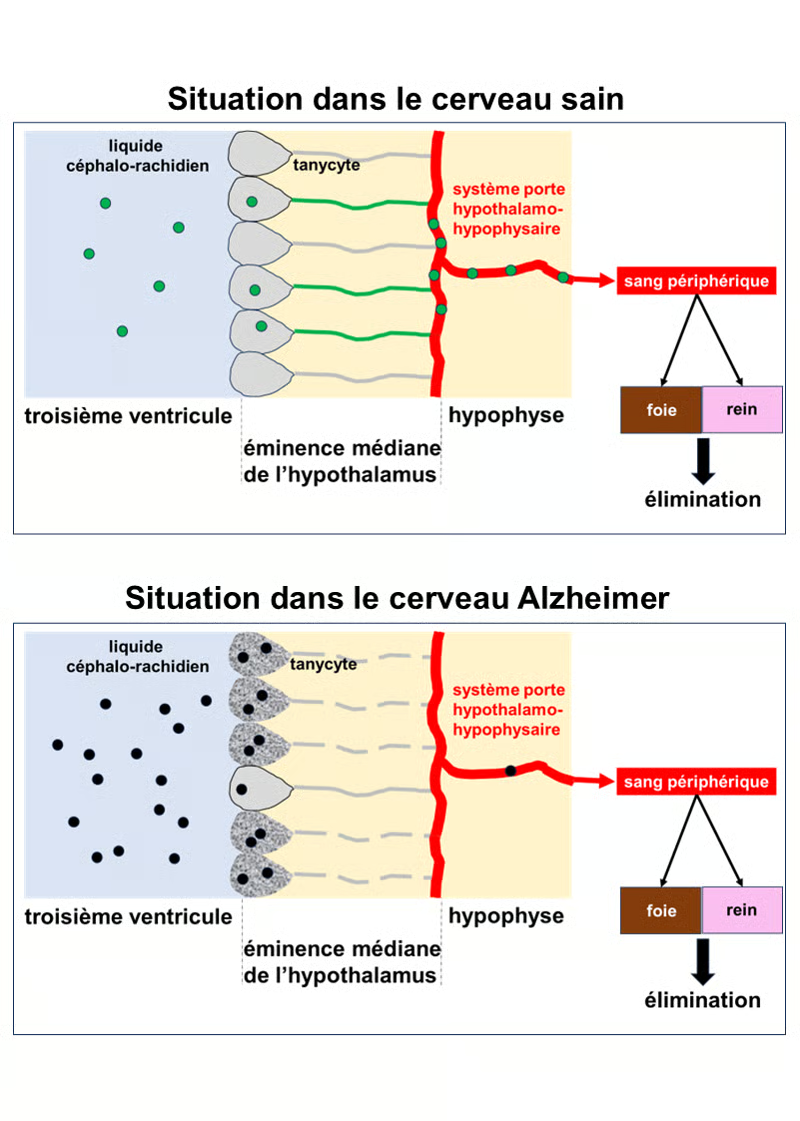
Résultats de l’étude
Partie haute : situation dans le cerveau sain. La protéine Tau normale schématisée par les cercles verts est présente dans le liquide céphalo-rachidien (bleu clair). Elle est captée par les tanycytes de l’hypothalamus qui tapissent le troisième ventricule du cerveau. Les tanycytes transportent la protéine Tau vers le sang via le système porte de l’hypophyse. Cette protéine est ensuite éliminée de l’organisme par le foie et le rein.
Partie basse : situation dans le cerveau Alzheimer. La protéine Tau est anormale et toxique. Elle est symbolisée par les cercles noirs. Dans le cerveau Alzheimer, les tanycytes sont dégradés et leurs prolongements qui assurent le lien avec le système porte de l’hypophyse sont fractionnés et donc non fonctionnels (pointillés gris). Ils peuvent intégrer la protéine Tau, mais ne peuvent l’exporter vers le sang et elle s’accumule dans le liquide céphalo-rachidien et le cerveau et poursuit son action toxique sur les neurones.
Peut-on réparer les tanycytes pour stopper la maladie d’Alzheimer ?
C’est aujourd’hui (mars 2026) impossible, mais cette stratégie reste un objectif des chercheurs. En trouvant des moyens de préserver la santé et l’intégrité des tanycytes, on pourrait maintenir le système d’élimination du cerveau de la protéine Tau (et d’autres) en état de fonctionnement, ce qui pourrait ralentir considérablement la progression de la maladie.
Pour aller plus loin
La protéine Tau
La protéine Tau est une protéine nativement non repliée, très soluble et thermostable, codée par le gène MAPT (microtubule-associated protein tau) sur le chromosome 17. Le cerveau humain adulte exprime six isoformes de cette protéine (352 à 441 acides aminés) générées par épissage alternatif : des combinaisons de 0 à 2 insertions N-terminales (0N/1N/2N) et de 3 ou 4 répétitions de liaison aux microtubules (3R/4R). L'isoforme la plus longue (2N4R, 441 acides aminés) est la plus fréquente.
Dans les neurones, cette protéine est associée aux microtubules (polymères de tubuline) qui sont les fibres constitutives du cytosquelette (sorte de voie ferrée sur laquelle transitent les molécules, protéines et organelles nécessaires à la vie et à la fonction des neurones) au niveau des axones et des dendrites. Une des principales fonctions de la protéine Tau est de stabiliser ces microtubules. Pour cela, elle se lie aux microtubules (avec une affinité d'environ 100 nM à des concentrations neuronales d'environ 2 μM), favorise la polymérisation de la tubuline, stabilise le réseau microtubulaire, et intervient dans le transport axonal, la morphologie neuronale, et le trafic intracellulaire. La protéine Tau est une phosphoprotéine.
Voici une liste de références sur cette protéine: Wang et al. Nature Reviews Neuroscience 2016; Chong et al. Cell and MolNeurobiol 2018; Shen et al. Cells 2025; Grundke-Iqbal et al., Proc Natl Acad Sci U S A. 1986; Hong et al. Biomolecules 2025; Wegmann et al. Curr Opin Neurobiol 2021.
Dans le cerveau normal, sa phosphorylation est régulée à un faible niveau (2 à 3 moles de phosphate par mole de tau) par un équilibre entre kinases (par exemple, GSK-3β, CDK5) et phosphatases (par exemple, PP2A). Ceci permet une fixation/détachement dynamique sans perturber la fonction. La protéine Tau normale reste monomérique/soluble et ne s'agrège pas. La fixation de ces groupes phosphates est étroitement contrôlée car elle impacte de façon critique la stabilité des microtubules.
Dans le cerveau Alzheimer, la protéine Tau subit une hyperphosphorylation anormale (3 à 4 fois supérieure à la normale, atteignant 6 à 8 moles de phosphate par mole de Tau, soit jusqu'à environ 39 à 45 sites phosphorylés dans la protéine Tau hyperphosphorylée). Parmi les sites clés figurent Ser202/Thr205, Thr231, Ser262, Ser396/404, etc. Ce phénomène est souvent associé à une activité réduite des phosphatases (par exemple, PP2A) et à une suractivation des kinases. La protéine Tau hyperphosphorylée se détache des microtubules, inhibe leur assemblage et provoque leur désassemblage. Elle séquestre la protéine Tau normale et d'autres MAP (microtubule-associated proteins, MAP1/MAP2) dans le cytosol.
Une fois détachée des microtubules, la protéine Tau se replie mal, forme des oligomères → des dimères → des filaments hélicoïdaux appariés ou des filaments rectilignes → des enchevêtrements neurofibrillaires insolubles à l’intérieur des neurones (au niveau du soma et des dendrites). Les six isoformes sont présentes dans les enchevêtrements neurofibrillaires. Des modifications supplémentaires, comme l’acétylation (par exemple, Lys280), la troncature (par exemple, au niveau d’Asp421 ou de Glu391 par les caspases) et l’ubiquitination, favorisent l’agrégation. Les formes oligomériques sont très toxiques et se propagent de manière similaire aux prions (ensemencement).
La protéine Tau hyperphosphorylée migre des axones vers les compartiment central et les dendrites. Les enchevêtrements neurofibrillaires endommagent les voies de transport de la protéine, induisent une inflammation, un dysfonctionnement synaptique et la mort neuronale. La présence des enchevêtrements neurofibrillaires est fortement corrélée au déclin cognitif et à la gravité de la maladie – souvent mieux que les plaques amyloïdes – et apparaît des décennies avant les symptômes.
On voit donc que dans un cerveau sain, la protéine tau est essentielle et protectrice lorsqu'elle est correctement régulée. Dans la maladie d'Alzheimer, l'hyperphosphorylation la transforme d'alliée en ennemie : elle perd son rôle stabilisateur et acquiert des propriétés toxiques qui entraînent la mort neuronale et la progression des symptômes. La protéine Tau est aujourd'hui une cible thérapeutique majeure (par exemple, les anticorps anti-Tau, les inhibiteurs de kinases), et des biomarqueurs comme la protéine Tau phosphorylée dans le liquide céphalo-rachidien ou l'imagerie TEP-Tau permettent, dans de nombreux cas, de mieux suivre l'évolution de la maladie, bien mieux qu’avec la seule protéine bêta-amyloïde.
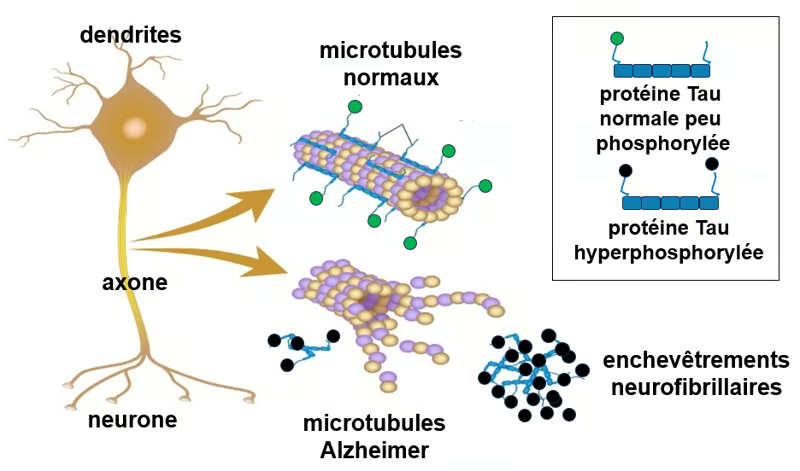
Figure. Protéine Tau et microtubules. L'une des principales fonctions de la protéine Tau est de moduler la stabilité des microtubules axonaux. Les axones et dendrites des neurones sont des parties très allongées de la cellule qui requièrent les microtubules comme soutiens structuraux et fonctionnels. Comme beaucoup d’autres protéines, la protéine Tau est sujette à des modifications notamment par liaison de groupes phosphates qui modifient sa fonction. Dans le cerveau humain adulte sain, la protéine Tau subit une phosphorylation physiologique (normale) sur un nombre limité de sites, soit en moyenne 2 à 3 groupements phosphate par molécule (protéine Tau symbolisée, porteuse d’un seul cercle de couleur verte). En revanche, dans le cerveau Alzheimer, la protéine Tau pathologique présente une hyperphosphorylation (souvent de 3 à plus de 10 groupes phosphates par molécule) sur de nombreux sites supplémentaires (symbolisée, porteuse de deux cercles de couleur noire), ce qui entraîne une diminution de son affinité pour les microtubules, une désorganisation des microtubules, son agrégation en enchevêtrements neurofibrillaires, conduisant à un dysfonctionnement et a la dégénérescence des neurones. Source : adapté de Alila Medical Media, Shutterstock.
L’hypothalamus et les tanycytes
L'hypothalamus est une petite structure du cerveau des vertébrés qui contient plusieurs noyaux aux fonctions variées. Chez l'humain, sa taille est comparable à celle d'une amande. L'une de ses fonctions est d'assurer la liaison entre le système nerveux central et le système endocrinien via l'hypophyse. Il contrôle ainsi la température corporelle, la faim, des aspects importants de la parentalité et des comportements d'attachement maternel, la soif, la fatigue, le sommeil, les rythmes circadiens et est important dans certains comportements sociaux, tels que les comportements sexuels et agressifs (Hypothalamus, Wikipedia).
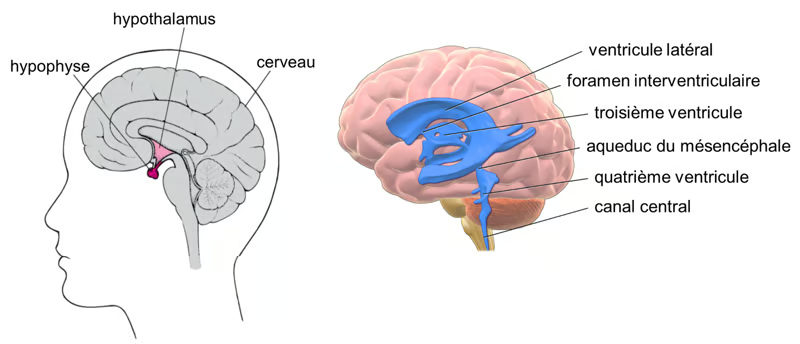
Figure. Hypothalamus et liquide céphalo-rachidien. A gauche position de l’hypothalamus et de l’hypophyse dans le cerveau. A droite les divers compartiments/ventricules dans lesquels se trouve le liquide céphalo-rachidien (Cerebrospinal fluid, Wikipedia). Sources : Manuel MCD et Bruce Blaus sous licence CC BY 3.0.
Les tanycytes sont des cellules gliales spécialisées de l’hypothalamus, localisées dans l’éminence médiane, qui tapissent le troisième ventricule (Mullier et al. J Comp Neurol 2010; Prevot et al. Handb Clin Neurol 2021; Elizondo-Vaga et al. J Cell Mol Med 2015; Rodriguez-Cortes et al. Trends Endocrinol Metab 2025; Balland et al. Cell Metab 2014; Imbernon et al. Cell Metab 2022; Fong et al. Front Neurosci 2023). Les tanycytes possèdent de longs prolongements qui entrent en contact avec les vaisseaux sanguins du système porte hypophysaire. Les tanycytes font ainsi office de pont - bidirectionnel - entre le liquide céphalo-rachidien et la circulation sanguine, comme le montre la figure ci-dessous.
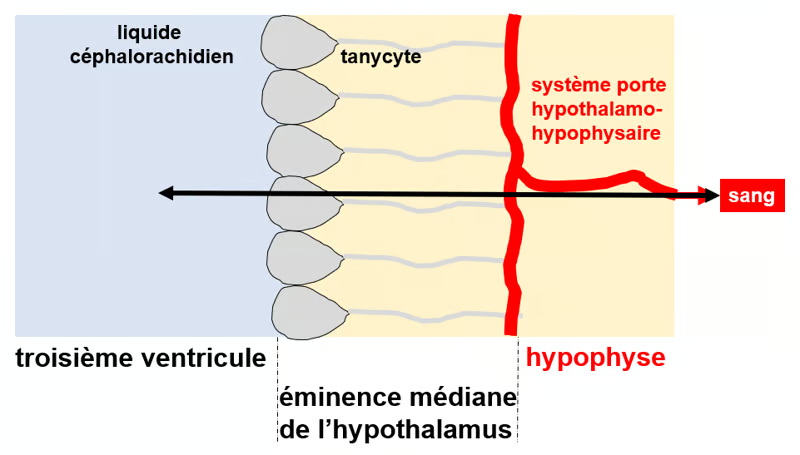
Figure. Les tanycytes comme moyen de transport entre le troisième ventricule et le sang périphérique. Les tanycytes sont constitués d’un corps cellulaire (gris entouré de noir à gauche) et de longs et fins prolongements (ligne grise). Les corps cellulaires tapissent les parois et le plancher du troisième ventricule (bleu clair à gauche), et les prolongements se terminent par des « pieds terminaux » en contact avec les capillaires fenêtrés (en rouge) du système porte hypothalamo-hypophysaire. Les tanycytes servent ainsi de pont entre le liquide céphalo-rachidien et la circulation sanguine périphérique.
Résultats de cette étude (Sauvé et al. Cell Press Blue 2026)
Quelques figures tirées de l'article sont présentées ici comme supports aux conclusions des auteurs.
- Des expériences sur des cultures cellulaires de rongeurs et des modèles animaux ont montré que les tanycytes transportent la protéine Tau du liquide céphalo-rachidien vers le sang.
- Le blocage de ce transport (par des procédures expérimentales appropriées) réduit cette élimination, entraîne une accumulation de la protéine Tau dans le liquide céphalo-rachidien et accélère/aggrave la pathologie.
- L'étude a également examiné les taux de protéine Tau dans les fluides corporels des patients. Chez les personnes atteintes de la maladie d'Alzheimer, les rapports plasma/LCR des protéines Tau totales et phosphorylées étaient diminués, ce qui concorde avec une altération de l'élimination de la protéine Tau du cerveau vers la circulation sanguine.
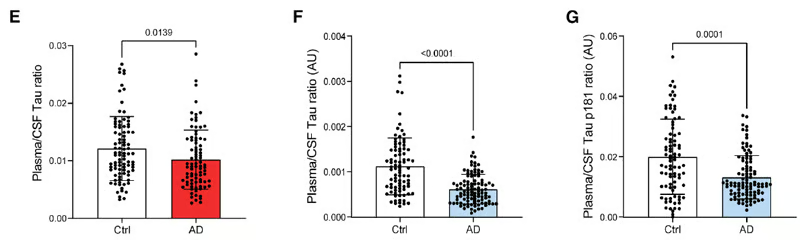
Figure 3 (E, F, G) de l'article de Sauvé et al. 2026. (E): Rapport entre le taux plasmatique (sang)/LCR de la protéine Tau chez les témoins (Ctrl) et les patients atteints de la maladie d'Alzheimer (AD), extrait de la base de données ADNI (témoins : n = 91 ; MA : n = 86). Les données ont été analysées par un test de Mann-Whitney bilatéral (U = 3077, p = 0,0139). Les résultats sont présentés sous forme de moyennes ± écart-type. (F) Rapport entre le taux plasmatique (sang)/LCR de la protéine Tau chez les témoins et les patients atteints de la maladie d'Alzheimer (AD), extrait de la cohorte BioCogBank (témoins : n = 86 ; MA : n = 104). Les données ont été analysées par un test de Mann-Whitney bilatéral (U = 2118, p < 0,0001). Les résultats sont présentés sous forme de moyennes ± écart-type. (G) Rapport entre le taux plasmatique (sang)/LCR de la protéine hyperphosphorylée Tau-181 chez les témoins et les patients atteints de la maladie (AD), extrait de la cohorte BioCogBank (témoins : n = 86 ; MA : n = 104). Les données ont été analysées à l'aide d'un test de Mann-Whitney bilatéral (U = 3051, p < 0,0001). Les données sont présentées sous forme de moyennes ± écart-type.
- Dans les tissus cérébraux post-mortem de patients Alzheimer, les tanycytes contiennent de la protéine Tau pathologique mais présentent une dégénérescence importante : leurs prolongements sont fragmentés/désorganisés. En conséquence, leur activité de transport de la protéine Tau est fortement diminuée.
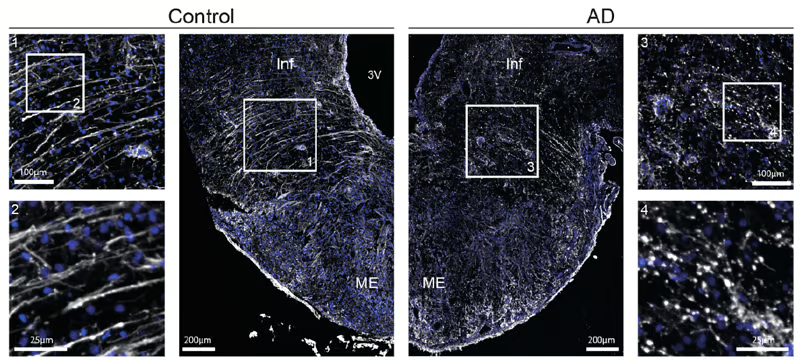
Figure 5 (A) de l'article de Sauvé et al. 2026. Photomicrographies de tanycytes dans l'éminence médiane de l'hypothalamus de témoins (à gauche, Control) et de patients atteints de MA (à droite, AD), marqués par immunofluorescence pour la vimentine (blanc). Encarts : images à plus fort grossissement des prolongements tanycytiques chez les témoins (encart 2 en bas à gauche) et les patients atteints de MA (encart 4 en bas à droite), montrant la fragmentation des prolongements chez ces derniers. La vimentine (qui apparaît en blanc) utilisée comme marqueur sur ces micrographies est une protéine exprimée dans les tanycytes.
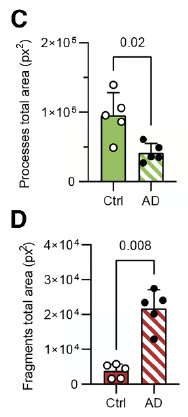
Figure 5 (C, D) de l'article de Sauvé et al. 2026. (C) Graphique représentant la surface totale couverte par les prolongements des tanycytes chez les témoins (Ctrl, n = 5) et les patients Alzheimer (AD, n = 5). Un test de Mann-Whitney bilatéral a été utilisé (U = 1, p = 0,02). Les données sont présentées sous forme de moyennes ± écart-type. (D) Graphique représentant la surface totale couverte par les fragments de prolongements de tanycytes chez les témoins (Ctrl, n = 5) et les patients Alzheimer (AD, n = 5). Un test de Mann-Whitney bilatéral a été utilisé (U = 0, p = 0,008). Les données sont présentées sous forme de moyennes ± écart-type.
- L'ensemble des données animales, cellulaires et humaines soutient l'existence d'une « navette tanycytaire » entre le cerveau et le sang, dont le dysfonctionnement pourrait accélérer l'accumulation de protéine Tau.
- Les auteurs ont tenté de comprendre pourquoi les tanycytes sont lourdement endommagés et non fonctionnels dans le cerveau des malades Alzheimer. Pour ce faire ils ont entrepris une étude du transcriptome (ensemble des ARNm) de ces cellules.
- Le séquençage des ARNm des tanycytes a révélé des modifications majeures, notamment : i) une sous-expression et une dérégulation des gènes impliqués dans le transport vésiculaire, l'ancrage et l'exocytose (sortie de la cellule), ii) une activation significative de diverses voies de réponse au stress cellulaire, et iii) au final le déclenchement de mécanismes de mort cellulaire.
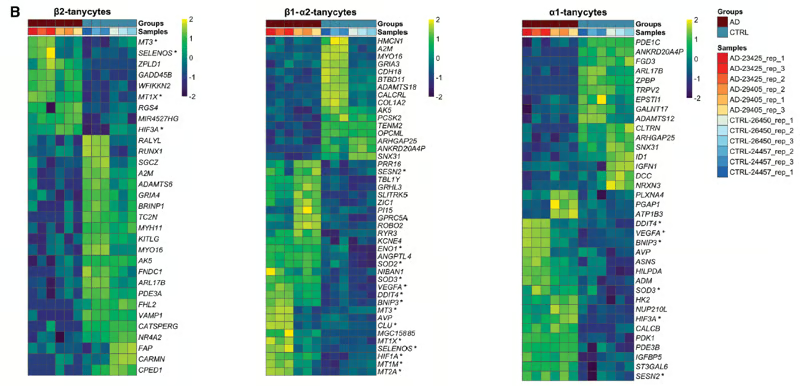
Figure 8 (B) de l'article de Sauvé et al. 2026. Carte thermique présentant les valeurs d'expression normalisées et mises à l'échelle par ligne des gènes différentiellement exprimés dans les tanycytes β2, β1/α2 et α1. Ces différents tanycytes sont localisés sur le troisième ventricule à des sites différents (Fong et al. Front Neurosci 2023). Les données ont été analysées à l'aide d'un test F de quasi-vraisemblance (QLF) comparant les comptages agrégés par échantillon, selon les conditions. Le seuil de signification a été fixé à un taux de faux positifs (FDR) ≤ 0,05. On voit très clairement sur cette figure que les gènes sont exprimés à des niveaux très différents entre les tanycytes issus de différents malades Alzheimer (barre marron en haut de la figure, AD) et ceux issus de cas témoins (CTRL); ces gènes sont généralement exprimés à un plus fort niveau pour la couleur jaune, et plus faible pour la couleur bleu foncée. Chaque ligne représente un gène différent dont le nom est placé à droite de chaque cadre.
- Cette dégénérescence altère la capacité des cellules à éliminer la protéine Tau du liquide céphalo-rachidien, entraînant son agrégation pathogène, sa propagation, son accumulation dans le cerveau, et contribue à la progression de la maladie d'Alzheimer.
Résumé de l’étude
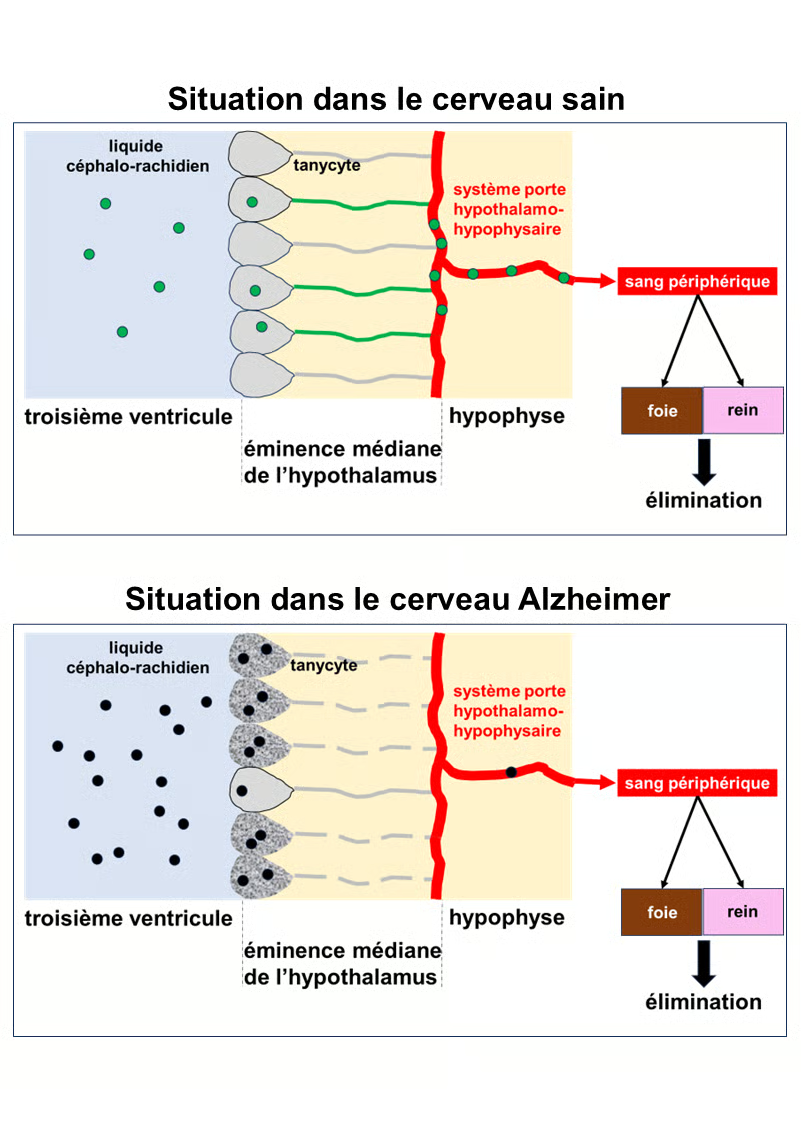
Partie haute : situation dans le cerveau sain. La protéine Tau normale schématisée par un cercle vert est présente dans le liquide céphalo-rachidien (bleu clair). Elle est captée par les tanycytes de l’hypothalamus qui tapissent le troisième ventricule du cerveau. Les tanycytes transportent la protéine Tau vers le sang via le système porte de l’hypophyse. Cette protéine est ensuite éliminée de l’organisme par le foie et le rein.
Partie basse : situation dans le cerveau Alzheimer. La protéine Tau est anormale et toxique (hyperphosphorylée). Elle est symbolisée par les cercles noirs. Dans le cerveau Alzheimer, les tanycytes sont dégradés et leurs prolongements qui assurent le lien avec le système porte de l’hypophyse sont fractionnés et donc non fonctionnels (pointillés gris). Ils peuvent intégrer la protéine Tau, mais non l’exporter vers le sang et elle s’accumule dans le liquide céphalo-rachidien et le cerveau et poursuit son action toxique sur les neurones.
Conclusion des auteurs
Cette étude met en lumière la fonction des tanycytes comme nouvelle cible thérapeutique potentielle dans le traitement de la maladie d’Alzheimer. Préserver ou restaurer leur intégrité pourrait améliorer l'élimination de la protéine Tau, ralentir la progression de la maladie et, au-delà, limiter les autres pathologies (démences) liées à la protéine Tau. Les chercheurs soulignent que le maintien de la fonction des tanycytes ne constitue probablement pas la seule solution à la maladie d'Alzheimer, mais pourrait représenter une nouvelle piste prometteuse. Cette étude recentre l'attention sur ce type cellulaire hypothalamique encore peu étudié comme acteur clé de la pathogenèse de la maladie d'Alzheimer, au-delà des visions neuronales ou amyloïdes traditionnelles.
Au-delà de l’implication des tanycytes dans la maladie d'Alzheimer, cette étude montre que ces cellules jouent un rôle important dans d’autres fonctions, notamment leur réponse supposée à divers facteurs de stress, leurs rôles mieux connus de transporteurs de signaux métaboliques et de régulateurs de la sécrétion d'hormones hypothalamiques.
Des études complémentaires devraient éclairer non seulement ce nouveau rôle dans les mécanismes d'élimination cérébrale, mais aussi dans la physiopathologie des maladies neurodégénératives.
A suivre...