Régression de la dengue par infection de moustiques Aedes aegypti mâles avec la bactérie Wolbachia
Résumé tout public
Le bon, la brute et le truand
Cette trilogie peut parfaitement s’appliquer au trio regroupant la bactérie, le moustique et le virus responsable de la maladie de la dengue.
Le moustique (la brute) pique l’humain et peut lui transmettre le virus (le truand) : l’humain tombe malade
La bactérie Wolbachia (le bon) infecte le moustique, bloque sa reproduction et la production du virus : l’humain n’est pas affecté
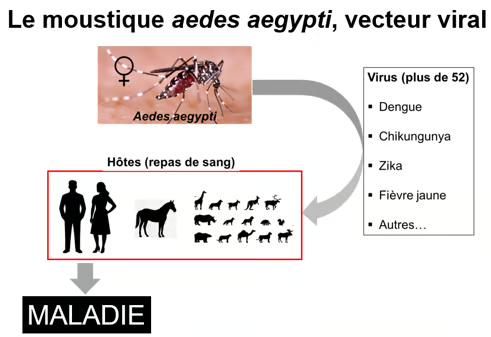
Figure. L'être humain est le principal hôte du virus de la dengue qui touche aussi d'autres mammifères. Une seule piqûre de moustique femelle infectée par le virus suffit à transmettre la maladie. Pendant les 2 à 10 jours suivant l'infection, le sang d'une personne infectée contient une forte concentration de particules virales. Lorsqu'une femelle moustique pique une personne infectée afin de se nourrir de son sang, le virus se propage à l'insecte, notamment au niveau de ses glandes salivaires. Lors de sa prochaine piqûre, le moustique injecte sa salive infectieuse dans le sang de sa victime, propageant ainsi la maladie. Le moustique Aedes aegypti est ainsi le vecteur de nombreuses maladies virales - pas seulement la dengue - comme indiqué sur la figure.
Brève histoire de la maladie
La dengue est une maladie virale véhiculée par les moustiques qui en ont été les hôtes ancestraux. Les primates non humains (Macaques et Presbytis) furent les premiers hôtes vertébrés du cycle sylvatique (forestier) à l'origine de la dengue moderne. Le moustique Aedes aegypti n'était pas le vecteur originel. Il a développé une forme spécialisée pour l'homme en Afrique de l'Ouest il y a des milliers d'années et n'est devenu le vecteur urbain dominant qu'après que le virus se soit déjà propagé depuis le cycle sylvatique. Les scientifiques estiment que la transmission à l'homme s'est produite il y a environ 500 à 2 000 ans (les estimations varient légèrement selon le sérotype et l'étude), une fois que les populations humaines en Asie et en Afrique sont devenues suffisamment importantes et denses pour permettre une transmission continue d'humain à moustique et de moustique à humain (https://www.nature.com/scitable/topicpage/dengue-viruses-22400925/).
Un article intitulé
"Suppression de la dengue par des moustiques mâles infectés par la bactérie Wolbachia" par Lim et al., vient d’être publié dans le New England Journal of Medicine le 26 mars 2026
Cette étude est basée sur le fait que les moustiques mâles Aedes aegypti infectés par la bactérie Wolbachia pipientis ne produisent pas de descendance après accouplement avec les femelles. Il s’agit d'un essai contrôlé-randomisé mené à Singapour, en milieu urbain, sur une période de 24 mois, portant sur une population estimée à environ 724 000 habitants. La ville a été divisée en 8 zones traitées (par lâchers de moustiques mâles infectés par la bactérie Wolbachia deux fois par semaine, environ 1 à 6 moustiques par résident et par semaine) et en 7 zones témoins (sans lâchers de moustiques) suffisamment distantes les unes des autres. Les cas de dengue symptomatiques confirmés en laboratoire (tous degrés de gravité et sérotypes confondus) ont été évalués à partir des données de surveillance nationale (RT-qPCR, antigène viral NS1, anticorps IgM, etc.).
La figure ci-dessous montre l’évolution de la population de moustiques femelles avant et après l’intervention.
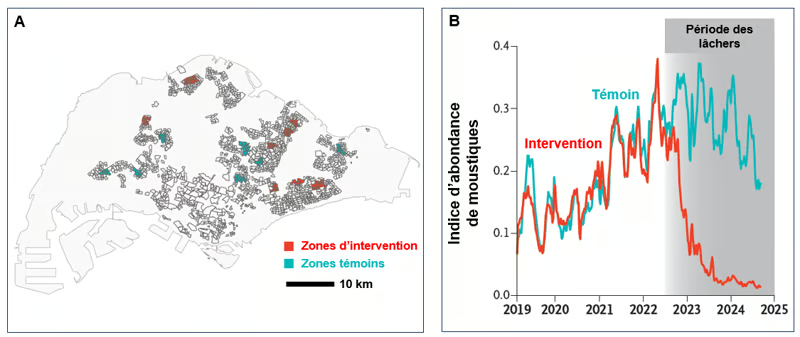
Figure. Population des moustiques Aedes aegypti dans des pièges randomisées. A. Plan de la ville de Singapour. Visualisation spatiale des zones d'intervention (rouge) et témoins (turquoise). B. Indice hebdomadaire d'abondance des moustiques adultes Aedes aegypti, mesuré à l'aire de pièges avant (témoin ligne turquoise) et pendant (intervention ligne rouge) le lâcher de moustiques mâles infectés par Wolbachia (période des lâchers en gris). L’indice est calculé en divisant le nombre total de moustiques femelles adultes Aedes aegypti capturés dans les pièges fonctionnels par le nombre de pièges fonctionnels (Adapté de Lim et al. NEJM 2026).
Les indices hebdomadaires d’abondance des moustiques avant l’intervention étaient similaires (environ 0,18–0,19). À partir de 3 mois après le lâcher des moustiques mâles infectés par la bactérie Wolbachia (et jusqu'à 24 mois), l'indice a chuté brutalement dans les zones d'intervention à 0,041, contre 0,277 dans les zones témoins, ce qui indique une suppression forte et durable de la souche sauvage d'Aedes aegypti. De plus, alors que le taux de résidents positifs pour la dengue dans les zones témoins était de 21 à 23 % pendant toute la durée de l’étude, ce taux est passé à 6-7 % chez les résidents des zones traitées, montrant une réduction du risque d'infection par la dengue d'environ 71 à 72 %.
A noter également que la bactérie Wolbachia inhibe fortement la réplication et la transmission du virus de la dengue chez le moustique A. aegypti contribuant encore à son effet bénéfique sur la transmission de la maladie (Voir ci-dessous).
Pour aller plus loin
La dengue
Cette maladie virale représente un problème majeur et croissant de santé publique dans les zones tropicales urbaines et suburbaines. On estime qu’aujourd’hui 400 millions de personnes sont touchées chaque année, et plus de la moitié de la population mondiale risque de contracter la maladie (https://www.pasteur.fr/fr/centre-medical/fiches-maladies/dengue). Sa forme bénigne évoque un syndrome grippal avec douleurs articulaires. Sa forme la plus sévère se manifeste par une fièvre hémorragique avec chute de tension artérielle extrême et un choc hypovolémique se développant brutalement, parfois quelques jours seulement après que la fièvre soit retombée. Ces symptômes constituent une urgence médicale, pouvant précéder une défaillance multiviscérale et le décès (Khan et al. J Infect Public Heath 2023; Wang et al. J Microbiol Immunol Infect 2020). S’agissant des vaccins contre le virus de la dengue, leur efficacité est généralement supérieure contre les formes graves que contre les formes bénignes et meilleure chez les personnes ayant déjà été exposées à la maladie. Aucun vaccin n'offre une protection à 100 % et le consensus actuel est que la maîtrise totale de la maladie nécessitera d’autres approches (Boscardin. Curr Top Microbiol Immunol 2026 ; Parra-Gonzalez et al. Front Cell Infect Microbiol 2025).
Le virus de la dengue et son vecteur le moustique Aedes aegypti
Le virus de la dengue, dont le nom scientifique depuis 2022 est Orthoflavivirus denguei (DENV), est un virus enveloppé à ARN monocaténaire de polarité positive appartenant au genre Orthoflavivirus. On connaît cinq variants différents de ce virus, notés DENV-1 à DENV-5. (Murugesan & Manoharan. Emerging and Reemerging Viral Pathogens. Chapter 16. 2020). Ce virus est transmis principalement par les moustiques Aedes aegypti, qui jouent un rôle de vecteur. L'être humain est le principal hôte du virus qui touche aussi d’autres mammifères. Une seule piqûre de la femelle du moustique suffit à propager l'infection si elle est porteuse du virus. Pendant les 2 à 10 jours suivant l'infection, le sang d'une personne infectée contient une forte concentration de particules virales. Une femelle moustique qui se nourrit de ce sang lors d’une piqûre, propage ensuite le virus dans les cellules tapissant son intestin. Au cours des jours suivants, le virus se propage aux glandes salivaires du moustique, et est libéré dans sa salive. Lors de sa prochaine piqûre, la femelle injecte cette salive infectieuse dans le sang de sa victime, propageant ainsi la maladie. De plus, le virus de la dengue peut persister dans les populations de moustiques par transmission transovarienne dans laquelle les moustiques infectés par le virus transfèrent le virus à leurs œufs (Vasilakis et al. Nat Rev Microbiol 2011). Le virus ne semble pas avoir d'effet néfaste sur le moustique, qui reste infecté à vie.
Origines ancestrales : d’abord, le cycle sylvatique
Les quatre sérotypes de la dengue qui infectent aujourd'hui l'homme (DENV-1 à DENV-4) ont évolué indépendamment à partir de souches ancestrales sylvatiques. Ces virus ancestraux circulaient dans un cycle primates non humains-moustiques dans les forêts d'Asie du Sud-Est (et séparément en Afrique de l'Ouest pour certaines souches). Les hôtes vertébrés étaient des singes (par exemple, des espèces des genres Macaque et Presbytis), et les vecteurs étaient des moustiques arboricoles (vivant dans la canopée) du genre Aedes – et non Aedes aegypti, comme c’est le cas aujourd’hui. On retrouve encore aujourd'hui des souches sylvatiques de DENV dans ces cycles forestiers et elles constituent la base de l'arbre phylogénétique pour les sérotypes humains. Ceci confirme que la transmission à l'homme s'est faite à partir du système primates-moustiques (Wang et al. J Virol 2000 ; Vasilakis et al. Nat Rev Microbiol 2011).
Les scientifiques estiment que la transmission à l'homme s'est produite il y a environ 500 à 2 000 ans (les estimations varient légèrement selon le sérotype et l'étude), une fois que les populations humaines en Asie et en Afrique sont devenues suffisamment importantes et denses pour permettre une transmission continue d'humain à moustique et de moustique à humain (https://www.nature.com/scitable/topicpage/dengue-viruses-22400925/).
La lutte anti-moustiques
Les mesures traditionnelles de lutte anti-moustiques (moustiquaires, protections individuelles ou pesticides, notamment) ont un impact limité ou contestable au plan écologique. Une mesure biologique, en cours d’utilisation depuis quelques années, est le contrôle de la population des moustiques Aedes aegypti par stérilisation aux rayons-X ou utilisation de la bactérie Wolbachia pipientis (Werren. Annu Rev Entomol 1997 ; Flores & O'Neill. Nat Rev Microbiol 2018 ; Werren et al. Nat Rev Microbiol 2008).
Deux techniques biologiques permettant de contrôler la population des moustiques sont à considérer ici :
La technique de l'insecte stérile par irradiation
Cette technique utilise l'irradiation aux rayons-X pour stériliser les moustiques mâles, qui sont ensuite relâchés en grand nombre pour s'accoupler avec des femelles sauvages, empêchant ainsi l'éclosion des œufs de ces dernières. Il s’en suit un déclin de la population sauvage au fil du temps et des lâchers successifs (Zhang et al. BMC Biol 2023).
La technique de l'insecte stérile par incompatibilité cytoplasmique
Dans cette technique, les moustiques sont élevés en laboratoire dans un environnement contenant la bactérie Wolbachia. Un point très intéressant à signaler ici est qu’en infectant les moustiques Aedes aegypti (mâles et femelles) la bactérie Wolbachia non seulement entraîne une stérilisation des mâles comme nous venons de le voir ci-dessus, mais également une inhibition dans les deux sexes de la réplication du virus de la dengue et d’autres virus dont ces insectes peuvent être porteurs (Flores & O'Neill. Nat Rev Microbiol 2018).
Deux stratégies peuvent être utilisées :
i) seuls les mâles sont relâchés et il y a alors suppression de la population sauvage. En effet, lorsqu'un moustique mâle infecté par Wolbachia s'accouple avec une femelle sauvage non infectée, ses œufs n'éclosent pas. L'effet est similaire à celui de la technique précédente et, avec le temps et des lâchers répétés, la population sauvage diminue.
ii) les deux sexes sont infectés par Wolbachia et relâchés dans l’environnement et il y a alors remplacement la population de moustiques sauvages.
Dans les deux cas, on aboutit à une situation dans laquelle la réplication du virus et donc la transmission de la maladie sont diminuées.
Des essais pratiqués ces dernières années dans divers pays tropicaux et notamment en Nouvelle Calédonie (ville des Nouméa et d’autres. https://www.worldmosquitoprogram.org/wmp-en-nouvelle-caledonie), ont montré que cette intervention réduisait le risque de dengue de façon significative (70%), mais l'efficacité protectrice de cette intervention variait selon les contextes géographique et humain (Zhang et al. BMC Biol 2023; Pinto et al. Plos Negl Trop Dis 2021; Utari et al. N Engl J Med 2021).
La bactérie Wolbachia et le mécanisme de l’incompatibilité cytoplasmique
Dans les testicules des moustiques, la bactérie Wolbachia modifie les spermatozoïdes en développement au niveau du complexe chromatine/nucléoprotéine paternel. Les spermatozoïdes matures contiennent généralement peu ou pas de bactéries Wolbachia, et la modification constitue donc une marque durable sur le spermatozoïde avant la fécondation. Cette modification perturbe le comportement normal des chromosomes paternels après la fécondation, provoquant souvent des problèmes de réplication de l'ADN, de condensation de la chromatine, de transition histone-protamine, de synchronisation mitotique ou de ségrégation chromosomique dans l'embryon précoce. Il en résulte un arrêt du développement embryonnaire. Pour plus de détail sur le mécanisme de l’incompatibilité cytoplasmique voir les articles suivants (Chen et al. Genes 2020 ; Hochstrasser. Annu Rev Microbiol 2022 ; Kaur et al. Plos Biol 2022 ; Zabalou et al. PNAS 2004; Sicard et al. Curr Opin Insect Sci 2019).
La bactérie Wolbachia inhibe de la réplication et la transmission du virus de la dengue chez A.aegypti
Non seulement Wolbachia stérilise le moustique mâle, mais de plus cette bactérie inhibe la réplication et la transmission du virus de la dengue (DENV) chez le moustique Aedes aegypti par de multiples mécanismes qui se conjuguent. Ces mécanismes ne sont pas encore entièrement élucidés, et différentes souches de Wolbachia (dont la souche wAlbB utilisée lors de l'essai de suppression à Singapour analysé ici) présentent des efficacités variables. Cependant, l'effet global est robuste : les moustiques infectés présentent des taux d'infection, de réplication et de dissémination du DENV vers les glandes salivaires, ainsi que de transmission à l'homme, nettement inférieurs. Ce blocage nécessite la présence de la bactérie et du virus dans la même cellule, et il est plus marqué lorsque la charge bactérienne de Wolbachia est élevée dans les tissus clés comme l'intestin et les glandes salivaires du moustique. Il affecte principalement les virus à ARN monocaténaire de polarité positive, comme le DENV, qui utilisent des compartiments de réplication membranaires cytoplasmiques pour leur réplication (Hussain et al. iScience 2023; Lu et al. Front Microbiol 2020; Bian et al. Plos Pathog 2010; Mushtaq et al. Front Immunol 2024).
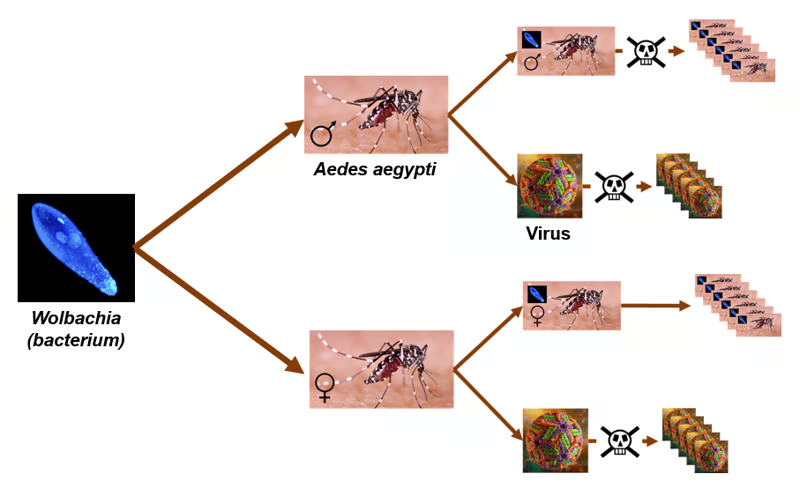
Figure. Les effets de Wolbachia sur le moustique A. aegypti. Partie haute de la figure: lorsqu'un moustique mâle s'accouple avec une femelle non infectée, l'embryon n'est pas viable (incompatibilité cytoplasmique) et la descendance est bloqué (stratégie de suppression de la population sauvage). Partie basse de la figure: lorsqu'un moustique mâle infecté s'accouple avec une femelle infectée, l'incompatibilité cytoplasmique est levée et la descendance est assurée (stratégie de remplacement de la population sauvage). Dans les deux cas, la production du virus DENV est également fortement diminuée.
Méthodes et expérimentations
Il s'agissait d'un essai contrôlé randomisé en zones géographiques, mené à Singapour, en milieu urbain dense, de 2022 à 2024. Les chercheurs ont divisé la ville sur 12 km² en 15 zones de logements sociaux de grande hauteur (population estimée à environ 724 000 habitants) d'environ 0,8 km² chacune, séparées par des distances suffisantes afin de limiter la propagation des moustiques. Huit zones (393 236 résidents) ont bénéficié de l'intervention ; sept zones (331 192 résidents) ont servi de témoins, sans lâcher de moustiques.
Des moustiques Aedes aegypti mâles (souche adaptée localement) infectés par la bactérie Wolbachia (souche wAlbB) ont été relâchés deux fois par semaine (environ 1 à 6 par résident et par semaine). Les lâchers ont utilisé une lignée locale présentant une incompatibilité cytoplasmique complète.
Critère d'évaluation principal
Les cas de dengue symptomatiques ont été confirmés en laboratoire (tous degrés de gravité et sérotypes confondus), et évalués à partir des données de surveillance nationale (RT-qPCR, antigène NS1, IgM, etc.). L'exposition à l'intervention était basée sur le groupe résidentiel (zone) et la durée (0, 3, 6, 9, 12 mois et plus). L'efficacité protectrice a été calculée à partir d'une régression logistique pondérée comparant les probabilités d'exposition chez les cas positifs et les cas négatifs à la dengue.
Suivi entomologique
L’indice hebdomadaire d'abondance des moustiques adultes femelles Aedes aegypti, a été calculé grâce aux pièges de capture d'intervention et de contrôle avant et pendant les lâchers de moustiques mâles infectés par Wolbachia. L’indice a été calculé en divisant le nombre total de moustiques femelles adultes Aedes aegypti capturés dans les pièges fonctionnels par le nombre de pièges fonctionnels. L'essai a été mené en parallèle avec la lutte antivectorielle intégrée standard dans les deux groupes et a été enregistré (ClinicalTrials.gov NCT05505682).
Résultats
Suppression de la population de moustiques
L’indice hebdomadaire d'abondance des moustiques initial était similaire (environ 0,18–0,19) dans les deux types de zones (intervention et témoin). À partir de 3 mois après le lâcher (et jusqu'à 24 mois), cet indice a chuté brutalement dans les zones d'intervention à 0,041, contre 0,277 dans les zones témoins, ce qui indique une suppression forte et durable de la souche sauvage d'Aedes aegypti.
Réduction de l'incidence de la dengue
Dans l'analyse en intention de traiter (après ≥ 6 mois d'exposition), 6 % des tests (354/5 722) étaient positifs à la dengue dans les zones d'intervention, contre 21 % (1 519/7 080) dans les zones témoins. L'efficacité protectrice était de 71 à 72 % sur des périodes d'exposition de 3, 6 et plus de 12 mois. Ces résultats ont été confirmés dans tous les sous-groupes (âge, sexe, année) et sont restés robustes aux analyses de sensibilité (par exemple, en excluant les tests IgM seuls). Le virus de la dengue de type 3 était prédominant. L'intervention a réduit à la fois la densité vectorielle et le risque de dengue chez l'humain en milieu urbain réel.
Conclusions et implications
Les auteurs concluent que des lâchers répétés de moustiques mâles Aedes aegypti infectés et stérilisés par le bactérie Wolbachia pipientis ont permis de supprimer efficacement les populations de moustiques et de réduire le risque d'infection par la dengue d'environ 71 à 72 % chez les résidents exposés de manière prolongée. Cette approche peut compléter les stratégies existantes de lutte antivectorielle et de vaccination et contribuer à réduire, voire à éliminer, la transmission de la dengue et d'autres maladies transmises par les moustiques du genre Aedes (par exemple, porteur des virus Zika et Chikungunya). L'acceptation du public s'est avérée élevée lors des essais pilotes précédents, et la méthode semble applicable à grande échelle en milieu urbain dense. Dans l'ensemble, cet essai randomisé à grande échelle, une des premières évaluations rigoureuses de lâchers exclusivement de moustiques mâles infectés par Wolbachia pour lutter contre la dengue, apporte des preuves solides de l'efficacité de cette méthode de suppression biologique.
Nouveautés apportées dans cet article
Cet article fournit à ce jour la preuve randomisée la plus solide que l’incompatibilité cytoplasmique (concernant les mâles infectés) due à l’infection par Wolbachia peut supprimer durablement les populations d’Aedes aegypti et réduire significativement le risque de dengue dans un environnement tropical urbain difficile et fortement touché. Il fait évoluer le domaine en validant la suppression de la population de moustiques (plutôt que son remplacement par des moustiques mâles et femelles infectés) comme un outil viable et potentiellement complémentaire, ne nécessitant pas l’établissement permanent de Wolbachia dans la nature. La conception et l'échelle de cette étude en font une référence en matière de politique opérationnelle de lutte antivectorielle. Les résultats obtenus permettent d'étendre cette approche à des contextes similaires et à d'autres maladies transmises par les moustiques Aedes.