Cellules souches et thérapie cellulaire
Un comité d’experts japonais approuve des produits médicaux à base de cellules souches pour traiter la maladie de Parkinson
TOKYO – Des experts du gouvernement japonais ont approuvé le 19 février 2026 des projets novateurs visant à fabriquer des « neurones médicaments » pour traiter la maladie de Parkinson. La thérapie cellulaire (baptisée Amchepry, développée par Sumitomo Pharma et Racthera Co, Ltd) basée sur l’utilisation de ces neurones, attend maintenant l'approbation finale du ministère Japonais de la Santé selon Kyodo News.
La maladie de Parkinson
Elle résulte de la dégénérescence progressive et sélective des neurones dopaminergiques. Ces neurones situés dans une région du cerveau appelée substance noire produisent et libèrent de la dopamine, un neurotransmetteur essentiel à la coordination des mouvements fluides et intentionnels. La dopamine influence également la motivation, la récompense et d'autres fonctions. Lorsque 50 à 80 % environ des neurones dopaminergiques disparaissent les symptômes moteurs classiques de la maladie de Parkinson apparaissent : bradykinésie (lenteur des mouvements), rigidité, tremblements au repos, instabilité posturale. La plupart des thérapies actuelles visent donc à compenser le déficit en dopamine soit, i) en stimulant sa production (administration de lévodopa), ii) en augmentant sa fonction (agonistes dopaminergiques), ou iii) en inhibant sa destruction. Il n'existe à ce jour aucun traitement curatif. C’est pourquoi de nouvelles approchent se mettent en place. Et l’une de ces approches est la thérapie à base de cellules souches.
Cellules souches
Les cellules souches sont des cellules non spécialisées qui constituent la « matière première » de l'organisme. Elles peuvent être décrites comme la source de tous les autres types cellulaires. Deux propriétés majeures les définissent : i) auto-renouvellement : elles peuvent se diviser et produire de nouvelles cellules souches identiques à elles-mêmes ; ii) différenciation : elles peuvent se développer (se différencier) en de nombreux types cellulaires spécialisés aux fonctions spécifiques, tels que les cellules musculaires, hépatiques, nerveuses, sanguines, osseuses ou cutanées. Les cellules souches agissent donc comme un système de réparation et de maintenance : elles remplacent les cellules mourantes, régénèrent les tissus, soutiennent la croissance et la cicatrisation tout au long de la vie de l’organisme.
On trouve des cellules souches dans les embryons (cellules souches embryonnaires qui vont générer le nouvel organisme), dans divers tissus adultes (cellules souches adultes ou somatiques, comme celles de la moelle osseuse ou de la peau). Elles peuvent également être créées en laboratoire (cellules souches pluripotentes induites ou cellules iPS).
Les cellules iPS
Le scientifique japonais Shinya Yamanaka a reçu le prix Nobel de Physiologie et Médecine en 2012 pour ses recherches sur les iPS, des cellules capables de se différencier en n'importe quel type de cellule du corps. Ces cellules sont créées en stimulant des cellules matures, déjà spécialisées, pour les ramener à un état juvénile – c’est à dire l’équivalent d’un clonage sans embryon. Ces cellules peuvent ensuite se différencier en divers types cellulaires et leur utilisation représente un axe majeur de la recherche médicale comme le montre la figure ci-dessous.
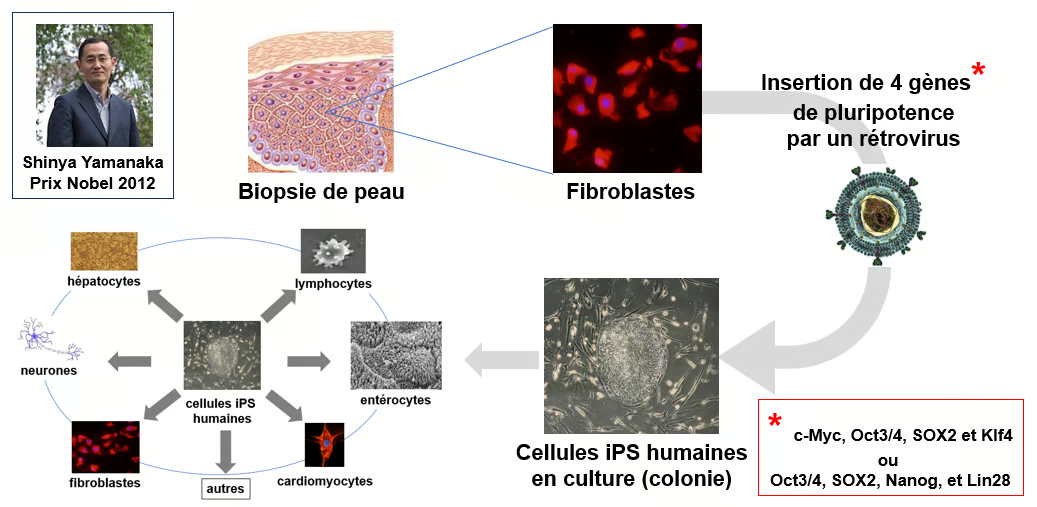
Figure. Génération de cellules iPS. Dans la méthodologie initiale mise en place par l’équipe de Yamanaka, les chercheurs utilisaient des cellules de peau (fibroblastes) de donneur comme point de départ. Les fibroblastes étaient cultivés dans un milieu liquide spécifique puis étaient transfectés par un vecteur rétroviral permettant l’insertion dans les cellules de quatre gènes dits de pluripotence, c’est à dire permettant la reprogrammation des fibroblastes vers un phénotype similaire à celui des cellules souches embryonnaires. On obtenait ainsi les cellules iPS. Ces cellules étaient alors mises en culture et soumises à un milieu de culture qui contenait les divers éléments nécessaires à leur différenciation vers divers types de cellules, hépatocytes, neurones, etc.
Thérapie cellulaire de la maladie de Parkinson par les cellules iPS
Ce projet de nouvelle thérapie a démarré en 2018. Nous avons vu plus haut qu’il attend maintenant l'approbation du ministère Japonais de la Santé. Il est basé sur une étude publiée en 2025 par Sawamoto et al. (Phase I/II trial of iPS-cell-derived
dopaminergic cells for Parkinson’s disease) dans la revue internationale Nature. La figure ci-dessous décrit les diverses étapes de cette thérapie.
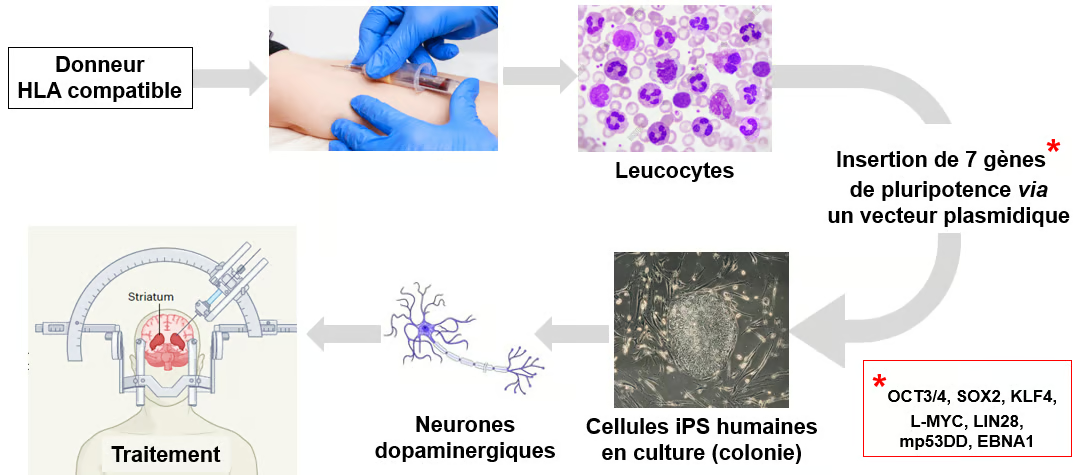
Figure. Thérapie cellulaire de la maladie de Parkinson par des cellules iPS. Les chercheurs ont constitué une banque de cellules de sang périphérique (leucocytes) issues de donneurs compatibles avec les groupes HLA majoritairement présents dans la population. Après leur mise en culture, ces leucocytes ont été transfectés par un vecteur plasmidique codant pour 7 gènes de pluripotence. Les cellules iPS obtenues ont alors été multipliées en culture et soumises à un processus de différenciation vers le phénotype de neurones dopaminergiques. Ces neurones ont ensuite été utilisées comme « cellules médicaments » et administrés sous contrôle stéréotaxique aux malades, au niveau du striatum, et les patients ont été placés sous médicament immunosuppresseur (Doi et al. Nature Communications 2020 ; Sawamoto et al. Nature 2025).
Les premières thérapies cellulaires utilisant des tissus fœtaux étaient prometteuses, mais présentaient des complications et des problèmes éthiques majeurs. Les cellules souches pluripotentes (iPS) représentent une alternative prometteuse pour le développement de traitements sûrs et efficaces. Dans cet essai clinique (jRCT2090220384) de phase I/II mené à l'hôpital universitaire de Kyoto, sept patients (âgés de 50 à 69 ans) ont reçu une transplantation bilatérale au niveau du striatum de progéniteurs dopaminergiques dérivés de cellules souches pluripotentes induites (iPS). Le striatum est une structure nerveuse subcorticale, double (droite et gauche), impliquée via le système dopaminergique dans le contrôle des mouvements, la motivation alimentaire ou sexuelle, la gestion de la douleur et la cicatrisation et la régénérescence de certains tissus cérébraux. Les critères d'évaluation principaux portaient sur la sécurité et les événements indésirables, tandis que les critères secondaires évaluaient l'évolution des symptômes moteurs et la production de dopamine pendant 24 mois. Aucun événement indésirable grave n'a été observé, et 73 événements indésirables légers à modérés ont été rapportés. Les doses de médicaments antiparkinsoniens des patients ont été maintenues, sauf en cas d'ajustement thérapeutique nécessaire. L'imagerie par résonance magnétique n'a révélé aucune prolifération excessive des cellules iPS greffées. Les auteurs ont également observé une diminution des symptômes moteurs : pendant que les participants prenaient leur traitement habituel, cinq des six participants inclus dans l'analyse d'efficacité ont montré une amélioration de la fonction motrice, et quatre ont bénéficié du maintien de cette fonction motrice après l'arrêt du traitement.
Conclusion des auteurs (Sawamoto et al.)
Bien que la sécurité et l'efficacité des produits cellulaires dérivés de cellules iPS continuent d'être étudiées, ces résultats suggèrent que la transplantation allogénique (provenant d’un donneur différent du malade) de progéniteurs dopaminergiques dérivés de cellules iPS est une thérapie régénérative sûre et efficace pour les patients atteints de la maladie de Parkinson. Les stratégies futures pourraient combiner la transplantation cellulaire avec la thérapie génique, les médicaments anti-Parkinson et la réadaptation afin d'en améliorer l'efficacité. De plus, la transplantation autologue utilisant des cellules iPS pourrait également constituer une option prometteuse.
Critiques et commentaires de la communauté scientifique
Globalement, la communauté scientifique considère ces résultats comme une preuve de concept encourageante pour la thérapie allogénique à base de cellules iPS, sûre et avec des signes d'activité biologique, mais sans preuve définitive suffisante et convaincante d'une efficacité robuste et cliniquement significative. Les experts (notamment dans Nature, News & Views, Brain et Parkinsonism & Related Disorders) suggèrent de façon unanime qu’un certain nombre de points doivent être abordés et réglés avant le lancement de futurs essais cliniques (Mullard Nature 2026) :
i) Seuls sept patients ont été traités (3 à faible dose, 4 à forte dose), avec des réponses variables (par exemple, des améliorations motrices chez 4 des 6 patients évaluables à 24 mois, mais pas chez tous). Les résultats pourraient ne pas être généralisables.
ii) Des études en double aveugle contrôlées par placebo sont nécessaires.
iii) Les réponses étaient inconstantes d'un patient à l'autre et les améliorations ne correspondaient pas toujours étroitement aux mesures de la production de dopamine.
iv) La survie et la fonction du greffon ont été évaluées jusqu'à 24 mois, mais la preuve définitive de la survie des neurones dopaminergiques matures n’a pas été apportée.
v) L'utilisation de cellules iPS allogéniques (provenant de personnes différentes des malades à traiter) soulève des questions d'extensibilité et d'immunité par rapport à l’utilisation de cellules autologues (cellules iPS produites à partir du malade lui-même) bien que ces dernières soient plus exigeantes en ressources.
Des essais cliniques menés en parallèle en 2025 utilisant des cellules souches embryonnaires humaines (Tabar et al. Nature 2025) avaient fait l'objet de critiques similaires.
A suivre donc...